生命编程:基因工程的奇迹与挑战
作者: 杨冬
在人类揭开自然界神秘面纱的征途中,基因工程已经从科幻小说中的幻想变成了现实中最令人心潮澎湃的科学实践。从古代农业中简单的育种选择到当代科学家对基因精准的编辑,人类对遗传技术的掌握已经实现了革命性的飞跃。
设想一下,如果我们能够更精准地操控生命的基础代码,那么治愈那些曾被认为是绝症的遗传疾病、大幅提升粮食生产效率、“定制”生物以满足工业需求……都将成为可能。同时,这些进步也带来了复杂的新挑战、新问题:基因工程将如何塑造我们的明天?在改善人类生活的同时,如何确保基因工程具备生物安全性、顺应社会伦理,从而避免潜在的负面影响?
基因工程缘起
自农业革命伊始,人类便投身于改变物种基因的伟大事业,这是一场历时弥久的探索。在古代,尽管先民们尚未掌握遗传学的深层规律,他们却凭借直观的观察,朴素地认识到某些生物特性能够从亲代传递至子代。简言之,他们对于“遗传”这一概念已有了初步的认识。基于对遗传现象的理解,先民们开始尝试通过筛选具有特定特性的个体进行配对,以此培养出符合人类需求的新品种。这一过程就是“人工选择”,它与英国生物学家达尔文所描述的“自然选择”相辅相成,共同成为驱动新物种形成和物种多样性的核心动力。在达尔文的经典著作《物种起源》中,他对这两种选择机制均进行了深入的探讨和阐释。正是得益于数千年的人工选择,人类得以成功培育出多样化的农作物和家畜品种,极大地丰富了我们的农业产出和生活资源。
遗传学的发展使育种技术进入了一个新的科学时代。虽然当时的人们尚未完全了解基因的本质,但遗传学的理论和方法已经极大地提高了人工选择的效率。除了传统的杂交技术,科学家们还开发出了诱变育种技术,利用化学物质或辐射诱发基因突变,并通过人工选择来培育具有特定特性的植物和动物。直到今天,许多重要的经济作物和家养动物,包括杂交水稻、观赏植物、肉鸡、家猪和奶牛等,都是通过人工选择培育出来的。然而,科学家们并不满足于此,他们开始思考:“如果我们能够直接操控基因,是否会创造出更适应人类需求的动植物品种呢?”
基因是什么
要实现直接操控基因这一目标,首先需要弄清楚基因到底是什么。20世纪中叶,科学家逐渐揭示了基因的本质—一段脱氧核糖核酸,简称DNA。随后,美国分子生物学家詹姆斯·沃森和英国生物学家弗朗西斯·克里克构建了DNA的双螺旋结构模型。基于这一发现,克里克进一步提出了中心法则,阐明了遗传信息从DNA到RNA(核糖核酸),最终传递到蛋白质的流动过程。也就是说,在生物体内,遗传信息被编码于DNA分子中,在机体需要时被转录至RNA,最后根据RNA上的信息合成蛋白质,这一过程被称为“翻译”。蛋白质在细胞中扮演着多种角色,如生物催化剂(酶)、细胞结构的构建成分(结构蛋白)及细胞信号分子等,它们是生物体功能和特性的决定性因素。中心法则的提出,为后续的遗传学研究奠定了基础。
随着人们对基因本质的理解进一步加深,如何精确操控基因成为科学界关注的前沿问题。20世纪50年代末,几项关键技术的重大突破为基因工程的发展奠定了坚实的基础。
科学家最先面临的挑战是如何获取并制备基因,这在本质上涉及合成DNA的过程。生物体内的DNA在细胞分裂前会自我复制,确保每个新细胞都得到一份完整的遗传信息副本。这一复制过程是由DNA聚合酶催化的。1958年,美国科学家阿瑟·科恩伯格发现了细菌的DNA聚合酶,并利用这一发现,在试管中成功合成了一段DNA,这是人类历史上首次实现 DNA的人工合成。进入20世纪80年代,凯瑞·穆利斯发明了聚合酶链式反应技术(PCR),该技术通过周期性地改变温度,模拟了DNA的自然复制过程。通过这一过程,目标DNA片段可以被指数级放大,从而在短时间内大量合成特定DNA,极大地提高了操控基因的效率和实用性。
成功获取基因后,科学家面临的挑战是如何将这些基因有效地引入细胞,并确保它们能在细胞分裂过程中稳定地传递。这一过程被称为基因克隆,它涉及一系列精密的科学步骤。
首先,我们需要一个基因载体—一种能够在细胞内自主复制的DNA片段。最常用的载体是经过改造的细菌质粒。质粒是细菌中的小型环状DNA,它们不仅能够自我复制,而且有一种让细菌细胞不得不保留它们的机制,即携带抗生素抗性基因。这种基因赋予细胞对特定抗生素的抵抗力,从而使其在含有抗生素的环境中更具生存优势。
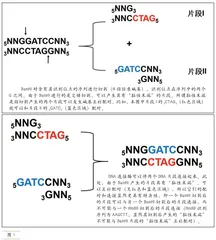
然而,即便有了载体,如何将目标基因嵌入其中仍是一个问题。这就需要用到限制性内切酶—一种能够识别并切割特定DNA序列的酶。BamHI就是一种限制性内切酶,它专门识别并切割DNA上的GGATCC序列(在G和G之间切割)。经BamHI切割后,DNA末端会形成特定的“黏性末端”,这些末端可以与相同限制性内切酶切割产生的末端形成稳定的连接(见图1)。假设我们有一个含有BamHI识别位点GGATCC的质粒和一个两端同样带有BamHI识别位点的目标基因,通过使用BamHI对两者进行切割,质粒就会变为线性质粒,而目标基因两端形成“BamHI黏性末端”。将这些切割产物混合,并加入DNA连接酶,就可以将目标基因的“黏性末端”与质粒的末端连接起来,形成一个新的闭合环状DNA分子(已包含了外源基因)。通过这种方式,外源基因得以整合进质粒载体,并可以被转入细胞,实现基因的克隆和表达。该技术的精妙之处在于,它不仅使我们能够将特定基因引入细胞,还能确保这些基因在细胞的生命周期中稳定传递。
科学实验或生产中使用的质粒载体一般都经过人工改造,在特定部位嵌入了多种不同的限制性内切酶识别位点,科学家便可以根据实验或生产的需要,选择恰当的限制性内切酶来精确切割基因和载体,实现精确的DNA操作。这一技术策略不仅能实现基因的克隆和表达,而且标志着DNA重组技术的重要进展。
在20世纪六七十年代,包括限制性内切酶和DNA连接酶在内的关键技术大多已经成熟,人类也具备了克隆基因的能力。在20世纪70年代末,基因工程领域迎来了向应用技术转向的契机。

基因工程正式启航
基因泰克(Genetech)作为首家上市的基因工程公司,标志着生物技术进入了一个新时代。该公司由重组DNA技术的先驱赫伯特·伯耶参与创立。基因泰克推出的首个产品是重组胰岛素,这是治疗糖尿病的革命性药物。
胰岛素是由胰岛分泌的激素,主要功能是降低血糖水平。对于1型糖尿病患者而言,由于胰岛功能受损,他们必须通过注射胰岛素维持血糖稳定。在重组胰岛素诞生之前,胰岛素的供应主要依赖于从动物体内提取。这种方式不仅成本高昂,而且由于动物胰岛素与人胰岛素之间存在氨基酸序列的差异,可能导致患者产生免疫反应,影响治疗效果。此外,从人类遗体中提取的胰岛素同样无法满足广泛的医疗需求。基因泰克公司利用基因工程技术合成的重组胰岛素不仅解决了供应问题,还极大地提高了治疗效果,成为糖尿病治疗史上的一个里程碑。
随着制药技术不断进步,制药公司对胰岛素基因进行了进一步的改造,通过引入特定的突变基因,开发出了具有改良特性的胰岛素。例如,甘精胰岛素通过在分子结构的特定位置用甘氨酸替代天冬氨酸,并增加两个精氨酸,延长了胰岛素的作用时间,为患者提供了更为便捷的治疗方案。这种通过改变蛋白质氨基酸序列来优化其生物性质的技术被称为蛋白质工程,这是基因工程领域的又一重要进展。
自重组胰岛素成功上市以来,一系列基因工程产品相继问世,广泛应用于医学领域。例如,生长激素、红细胞生成素和粒细胞集落刺激因子等已经成为治疗相关疾病的有效药物。然而,并非所有基因工程产品都达到了预期的临床效果。例如,白细胞介素2是一种在免疫细胞成熟过程中发挥关键作用的细胞因子,尽管初步研究显示白细胞介素2具有抑制肿瘤生长的潜力,但由于副作用难以控制,其临床应用仍然受限。另一个例子是干扰素,这是一种具有广泛抗病毒活性的细胞因子。基因工程合成的干扰素在治疗某些病毒性疾病和恶性肿瘤方面已显示出显著疗效,但要实现将其变为“万能药”的长远目标,仍有很长的路要走。
以上提及的基因技术通常涉及利用基因工程使宿主细胞(通常是细菌,有时也包括酵母)产生具有药用价值的蛋白质。随着技术的进步,现在科学家可以在一个细胞内引入多个外源基因,并通过突变来调节宿主细胞基因的表达水平,从而改变细胞的代谢途径,促使其合成特定的化学分子。这种技术被称为代谢工程技术,可以视为基因工程的高级形式。在这一领域,美国科学家杰伊·基斯林取得了令人瞩目的成就。他在酵母细胞中引入了编码两种酶的基因,这两种酶能够合成青蒿酸;通过进一步的基因操作,提高了青蒿酸前体化合物的合成效率,并减少了其消耗。通过发酵过程,改造后的酵母可大量生产青蒿酸,再通过化学反应将青蒿酸高效转化为青蒿素,从而大大降低了青蒿素的生产成本,为疟疾治疗做出了重大贡献。
从植物到动物的遗传改良
起初,基因技术主要聚焦于微生物细胞领域的应用,随着研究逐步深入,其触角已经远远超出微生物领域。现在,基因工程被广泛地应用于植物和动物的遗传改良,极大地丰富了生物技术的内涵。
植物的基因工程
抗虫玉米
植物转基因技术的一个关键工具是根癌农杆菌,这是一种在自然环境中能够引发植物肿瘤的细菌。根癌农杆菌携带有一个名为Ti的质粒,质粒中包含一个特殊的DNA片段—T-DNA。当植物遭到损伤时,根癌农杆菌便会趁机从伤口处侵入植物组织,并将T-DNA注入植物细胞内,并将其整合入植物的基因组中。T-DNA上的基因表达会促使植物细胞增殖,形成肿瘤。在基因工程领域,科学家们会将目标外源基因插入T-DNA,利用根癌农杆菌这一特性,实现植物的转基因。
20世纪80年代,基因工程技术迎来了一个重要的里程碑—第一种抗虫害玉米问世。通过转基因技术,这种玉米拥有了苏云金杆菌毒素基因,通常情况下,该毒素在苏云金杆菌孢子中以晶体形式存在。这些晶体被特定昆虫(如鳞翅目、鞘翅目和双翅目昆虫)摄入后,会在昆虫消化道的碱性环境中溶解,溶解后的毒素则会与昆虫消化道细胞的特定受体结合,破坏昆虫肠道的完整性,导致昆虫死亡。此外,苏云金杆菌毒素展现出的高度专一性意味着它对特定昆虫具有杀伤力,对哺乳动物则无毒性,因此,苏云金杆菌毒素常被用作生产生物农药。随着植物基因工程技术的发展,通过使玉米表达这种毒素的特性,科学家成功培育出了具有抗虫害特性的转基因玉米。这不仅提高了作物产量,还有助于减少化学农药的使用,对环境保护具有重要意义。
继成功培育出抗虫害玉米之后,科学家利用苏云金杆菌毒素基因进一步开发了抗虫害棉花、土豆、西红柿和水稻等作物。这项技术的广泛应用提升了作物产量,也减少了农民对化学农药的依赖。然而,这些转基因作物的推广也引发了一些争议。
首先,人们担心昆虫可能逐渐对苏云金杆菌毒素产生耐受性,这可能会降低转基因作物的抗虫效果。这是农业科学家们长期、密切关注的问题。其次,人们担忧苏云金杆菌毒素可能对非目标昆虫造成伤害。1999年,有报道指出,转基因玉米的花粉可能污染了帝王蝴蝶的食物来源—马利筋(一种北美地区常见的草本植物),从而对这种蝴蝶的生存构成威胁。尽管后续研究认为转基因玉米对帝王蝴蝶的影响微乎其微,但这类作物对生态系统造成的长期影响仍需要进一步研究。再次,关于苏云金杆菌毒素的人体安全性也存在疑问。尽管目前的研究显示,这种毒素对哺乳动物无毒,但公众对其是否可能引起过敏反应以及苏云金杆菌的基因是否会通过消化系统转移至人体细胞中仍存有疑虑。不过,现在还没有足够的研究证据证明转基因植物会造成以上提及的种种问题。