高考综合实验试题在化学教学中的引导作用和育人价值
作者: 周琦 张霞丽 赵桂 周东
摘要: 将高考综合实验试题与实验教学相结合,一方面,通过深度研析高考试题,可以促使教师更加精准地把握教学内容,进而对教学思想和教学方法进行补充和调整;另一方面,对高考实验试题进行实验还原及探究,也可以充分调动学生的积极性和参与热情,促进学生化学学科核心素养的培养。通过对2020年全国Ⅱ卷中27题深度研习并以此为基础开展探究式实验教学,探索高考试题在卷面之外的作用,进一步发挥高考试题引导教学的功能,充分展现其育人价值。
关键词: 高考综合实验试题; 实验探究; 化学学科核心素养
文章编号: 10056629(2022)10008805
中图分类号: G633.8
文献标识码: B
1 问题的提出
高考综合实验试题注重从不同的角度考查学生的化学学科核心素养,同时发挥高考的育人功能和积极的导向作用[1~3]。对高考综合实验试题进行解析、还原与再探究,有助于引导学生在学习科学知识的同时加深思考和反思,促进知识向能力和素养的转化。同时在实验教学中,对教学目标的确定、情景素材的选取、课堂问题的设计、教学评价等均具有重要的参考价值,教师以化学高考试题引导学生进行实验探究,能够使学生带着求知欲和好奇心去探究化学学科知识。更为重要的是,将高考综合实验试题与平时的实验教学结合起来能够使学生通过化学实验了解化学学科知识产生的过程,体会化学家们探索化学知识的科学思维和过程,有助于培养学生严谨求实的科学态度。本文以2020年全国Ⅱ卷中27题为例,对试题本身进行深度研习并以此为基础进行试题还原的探究式实验教学,以期为一线教师充分利用高考试题资源提升学生化学核心素养提供参考。
2 试题解析,挖掘考题背后的育人价值
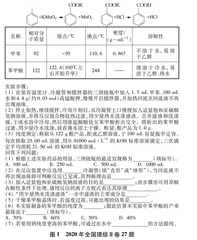
高考综合实验试题注重考查化学学科核心素养,能有效培育学生的逻辑推理、信息加工及知识迁移运用的能力。以2020年全国Ⅱ卷第27题“苯甲酸的制备及分析”(见图1)为例进行分析。
苯甲酸可用作食品防腐剂。实验室可通过甲苯氧化制苯甲酸,其反应原理简示如下:
实验步骤:
(1) 在装有温度计、冷凝管和搅拌器的三颈烧瓶中加入1.5 mL甲苯、100 mL水和4.8 g(约0.03 mol)高锰酸钾,慢慢开启搅拌器,并加热回流至回流液不再出现油珠。
(2) 停止加热,继续搅拌,冷却片刻后,从冷凝管上口慢慢加入适量饱和亚硫酸氢钠溶液,并将反应混合物趁热过滤,用少量热水洗涤滤渣。合并滤液和洗涤液,于冰水浴中冷却,然后用浓盐酸酸化至苯甲酸析出完全。将析出的苯甲酸过滤,用少量冷水洗涤,放在沸水浴上干燥。称量,粗产品为1.0 g。
(3) 纯度测定:称取0.122 g粗产品,配成乙醇溶液,于100 mL容量瓶中定容。每次移取25.00 mL溶液,用0.01000 mol·L-1的KOH标准溶液滴定,三次滴定平均消耗21.50 mL的KOH标准溶液。
回答下列问题:
(1) 根据上述实验药品的用量,三颈烧瓶的最适宜规格为__________(填标号)。
A. 100 mL B. 250 mL C. 500 mL D. 1000 mL
(2) 在反应装置中应选用__________冷凝管(填“直形”或“球形”),当回流液不再出现油珠即可判断反应已完成,其判断理由是__________ 。
(3) 加入适量饱和亚硫酸氢钠溶液的目的是__________ ;该步骤亦可用草酸在酸性条件下处理,请用反应的离子方程式表达其原理 __________ 。
(4) “用少量热水洗涤滤渣”一步中滤渣的主要成分是__________ 。
(5) 干燥苯甲酸晶体时,若温度过高,可能出现的结果是__________ 。
(6) 本实验制备的苯甲酸的纯度为__________;据此估算本实验中苯甲酸的产率最接近于__________(填标号)。
A. 70% B. 60% C. 50% D. 40%
(7) 若要得到纯度更高的苯甲酸,可通过在水中__________ 的方法提纯。
该试题综合性突出,以合成常见的食品添加剂苯甲酸为载体,涉及反应、加热、搅拌、冷却、过滤、除杂、干燥、纯度分析等操作,多角度地考查了学生的基本实验技能和综合实验能力。解决真实问题是培养学生高阶思维和创新能力,发展和检验化学学科核心素养的重要方式。
3 试题还原与探究,发展核心素养
3.1 试题还原,促进知识向学科能力的转化
为了更深入地研究此试题,在教师的帮助下让学生在实验室按照图1高考试题方法(以下简称原始实验)进行还原重复实验。重复实验过程中约2小时油珠消失,制得的苯甲酸粗产品为1.1g,产率为56%,纯度为87%,与试题所给数据基本一致。实践证明,对原始实验进行还原有助于学生学会:(1)设计合理、可行的实验方案;(2)正确选用实验装置;(3)掌握控制实验条件的方法;(4)预测或描述实验现象、分析或处理实验数据,得出合理的结论;(5)评价或改进实验方案等综合实验能力的提升。
3.2 引导学生发现问题,发展“证据推理与模型认知”核心素养
重复实验中按照原始方案制得的苯甲酸纯度为86%,是什么因素影响了产物的纯度,有没有方法提高产物的纯度?这一问题是在已有实验结果上的“生长”,学生可以根据已有知识做出合理的解释。同时此问题有效激发了学生对实验做进一步探究的积极性,师生在实验室围绕这一问题展开了一场热烈的讨论。部分对话记录如下:
[师]请同学们结合所学的混合物的分离和提纯、乙醇的性质、酸碱中和滴定等实验经验来讨论苯甲酸纯度为86%的可能原因及提高纯度的方法。
[生1]我觉得水浴干燥得不彻底,苯甲酸中含有少量的水分,可以用一个其他实验仪器或方法延长干燥的时间,将苯甲酸干燥得彻底些。
[生2]我觉得是KOH溶液的浓度太小了,很容易与空气中的CO2反应,引起较大的误差。可以换用浓度约为0.1mol·L-1的NaOH溶液进行实验。
[生3]滴定过程中用到容量瓶和移液管两个量器是不是会增大误差,有没有其他更科学的方式还需要老师指导。
[生4]产品在洗涤环节中可能洗涤得不彻底,可能含有无机盐。用离子来表示的话阴离子可能有Cl-、 SO2-4,根据电中性原理阳离子可能有Na+、 K+、 Mn2+。阴离子可以用AgNO3溶液和BaCl2溶液进行检验,阳离子Na+、K+可以用焰色反应进行检验,但Mn2+不知道怎么检验。
[生5]在有机化学里曾学习过乙醇的性质,乙醇跟金属钠反应会产生氢气,感觉乙醇有弱酸性,使测得的结果有些偏大。
[师]同学们的思维非常活跃,合成的物质中含有水分确实会降低其纯度,可使用实验室常见的恒温干燥箱将新制的苯甲酸干燥到恒重即可除去游离的水分。确实实验室最常用的是浓度约为0.1mol·L-1的NaOH溶液。在大学分析化学中用减量法称取药品加溶剂溶解再滴定,可以避免使用容量瓶跟移液管两种量器以减小实验误差。阳离子Na+、 K+用焰色反应来鉴别的话需要离子的浓度较大,且不能定量,大型仪器电感耦合、荧光光谱等离子光谱仪可以检测Na+、 K+、 Mn2+的含量。至于乙醇有没有酸性,可以做个空白对照试验验证。请同学们根据讨论的结果进行实验探究。
从学生熟悉的实验及实验原理出发,引导学生进一步推理,促使学生将已有的知识迁移应用到新的情境中,从而寻找到解决问题的方法,发展“证据推理与模型认知”核心素养。教师通过引导学生以“证据推理”的方式学习影响苯甲酸纯度的因素,提示学生从混合物的分离和提纯、乙醇的性质、酸碱中和滴定等方面进行思考。学生由影响苯甲酸纯度的因素结合已有的科学知识及实验经验出发,多数能想到影响物质纯度的因素有:含有水分、无机盐(洗涤不彻底)。优生还可能会想到两个量器同时使用会产生系统误差以及溶剂乙醇上羟基H的性质等。通过乙醇分子结构的理论知识进行推断,有助于学生对“宏观辨识与微观探析”这一化学学科核心素养的更深层次的理解。同时教师给学生普及现代大型分析仪器知识,有助于开拓学生的视野。
3.3 探究影响纯度的因素,发展“科学探究与创新意识”核心素养
学生在教师的引导下设计实验方案、开展实验、得出结论才能完整地体会实验探究过程。
[师]同学们根据讨论推理的结果设计了实验方案并进行了实验,请同学们说说苯甲酸纯度为86%的原因,实验探究的过程和实验现象及结论。
[生]取水浴干燥以后的苯甲酸0.9775g放在95℃恒温干燥箱里进行干燥,直到重量不再变化(干燥至恒重),重量为0.8692g。说明沸水浴干燥并不彻底,所得粗产品中仍含有约10%的水,这是影响产品纯度的主要原因。
[生]接着对已完全干燥的苯甲酸粗品按原始实验的步骤进行纯度分析:称取0.1225g粗产品,配成乙醇溶液,于100mL容量瓶中定容。每次移取25.00mL溶液,用已标定的0.0123mol·L-1的KOH标准溶液滴定,三次滴定平均消耗19.89mL的KOH标准溶液,通过计算得到已干燥的苯甲酸粗品的纯度高达97.4%。
[生]做了乙醇的空白对照试验,移取25.00mL乙醇于锥形瓶中,加入2滴酚酞指示剂,消耗0.0123mol·L-1的KOH溶液1.15mL,该实验证明直接使用乙醇确实会影响产物的纯度,使得纯度偏大。
[生]又取少量的产品加入适量的蒸馏水温热溶解,将溶液分为两份,一份向里面加入足量稀硝酸,无明显现象,再加入两滴AgNO3溶液,产生白色沉淀,说明苯甲酸的粗品中含有Cl-;另一份向其中加入足量稀盐酸,无明显现象,再加入BaCl2溶液产生白色沉淀,说明苯甲酸的粗品中含有SO2-4。此外,根据溶液的电中性原理,此粗产物中可能含有K+、 Na+、 Mn2+等阳离子。这些实验说明粗产品中还含有少量无机盐,这也是影响产品纯度的原因之一。
[师]同学们通过实验证明了高考题中苯甲酸的纯度低主要是由于在沸水浴上苯甲酸干燥不彻底依然含有水分以及苯甲酸粗品没有洗涤干净含有少量的无机盐两个原因共同造成的。
通过讨论影响纯度的因素,学生根据讨论的结果设计了实验方案,并对自己提出的假设进行了实验验证,通过假设、实验、推理和评价等系列活动,有效锻炼了学生的化学思维能力和化学实验能力,发展学生“科学探究与创新意识”的核心素养。
3.4 问题拓展,激发强烈的求知欲
按照原始方案制得苯甲酸的产率约为50%,是什么影响了产率?能否进行改进?这一问题的设置是在原始实验基础上的提升,需要教师课前查阅相关资料并进行预测。对原有实验进行拓展可以进一步激发学生的探索精神,有助于在更高层次上培养学生的“科学探究与创新意识”。
[师]按照原始方案制得的苯甲酸产率约为50%,请结合苯甲酸在冰水中的溶解度(约为0.18g)、甲苯在水中的溶解度[0.11g(0.13mL)/100mL(100℃)、 0.047 g(0.05mL)/100mL(16℃)],分析是什么影响了产率,能否进行改进?
[生1]我觉得和水的用量有关。水多了,高锰酸钾的浓度变小了,高锰酸钾的氧化能力变弱了,甲苯没有氧化完全,在合成过程中减少水的用量。
[生2]我觉得是溶液中的水太多,一开始就加入了100mL,后面又加入饱和亚硫酸氢钠溶液又会引入水将苯甲酸钾的母液稀释,导致在酸化的过程中苯甲酸有一部分溶解在了水里,没有析出,减少溶剂水的用量,减小苯甲酸溶解在水里的质量,优化实验中可考虑加入亚硫酸氢钠固体不会引入水。