浓硫酸与铜反应实验改进
作者: 岳倩 曾春梅
摘 要:针对现有教材中浓硫酸与铜反应实验装置的不足,如易倒吸、尾气未处理尽等进行改进:使用定制的双边具支试管作为该反应装置、性质检验装置以及净化装置,
用硅胶塞代替橡胶塞,铜丝可以轻松穿过。避免了橡胶塞打孔使气密性良好。换用棉团浸取试液,可减少药品用量且效果良好。改进后的装置能有效检验二氧化硫的还原性、酸性以及漂白性,具有现象明显、无污染、防止倒吸等优点。
关键词:浓硫酸与铜反应;实验改进;双边具支试管
文章编号:1005-6629(2024)09-0071-03
中图分类号:G633.8
文献标识码:B
1 问题的提出
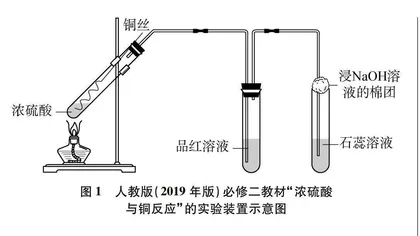
铜和浓硫酸的反应及实验在高中化学学习中占有重要地位,是认识浓硫酸的氧化性和酸性的重要载体。同时,作为二氧化硫的制备与性质检验实验,能够让学生进行关于有害气体的制备与检验的系统化学习。二氧化硫和硫酸作为硫的重要化合物所呈现出来的特殊性质,有助于学生深入认识化合价与物质性质之间的联系,从而掌握物质结构决定性质的本原知识。人教版教材(2019年版)必修二[1]中设置的铜与浓硫酸反应实验(如图1所示),存在些许不足:(1)铜丝和橡胶塞之间的摩擦力较大,不易抽拉铜丝,操作困难,容易损坏试管;(2)用一个浸有氢氧化钠溶液的棉团来吸收多余的二氧化硫是不严谨的,
因为产生的二氧化硫较多、较快,很容易逸出;(3)装置内残留的二氧化硫未处理,拆卸装置时也会逸出;
(4)没有设计防倒吸装置,停止加热时,品红溶液会倒吸进入反应试管中;(5)探究了二氧化硫的漂白性,但未进一步验证其漂白效果的不稳定性,而且二氧化硫的还原性也未检验,这些问题都会让学生感到疑惑。因此,笔者结合文献对
铜与浓硫酸反应的实验装置进行了再改进。
2 相关文献案例评析
基于图1实验装置的弊端,不少研究者对其进行了改进,在此不妨简单分析一下几类具有代表性的改进实验方案。
方案一[2]:利用洗耳球排出装置内残留的SO2;使用品红试纸和石蕊试纸检验SO2;使用80%的硫酸,使容易观察到蓝色硫酸铜溶液的生成;铜丝通过胶头滴管插入具支试管,减小了铜丝与胶帽之间的摩擦力。不足之处是:(1)将胶头滴管穿过橡胶塞的操作过于困难,且很难保证装置的气密性;(2)加热硫酸过程中会产生大量酸雾进入到双通管里,会使石蕊试纸变色,从而干扰SO2的酸性检验。
方案二[3]:通过条形磁铁吸引铁钉,能控制反应的进程,增加实验的趣味性;将球形干燥管伸入到氢氧化钠溶液中,可以充分吸收SO2,平衡气压,防止倒吸。不足之处是:(1)缺少检验SO2酸性的装置;(2)高温下,铁钉与浓硫酸酸雾接触也会反应;(3)条形磁铁需要全程用手控制,操作不便;(4)反应装置里残留的SO2未处理;(5)反应后的液体不易呈现明显的蓝色。
方案三[4]:使用Y形管实现了装置一体化;使用单向阀、双球安全漏斗等能除去残留的SO2和防倒吸。不足之处是:(1)不能控制反应的进程,在低温时发生较多副反应,生成黑色物质;(2)缺少SO2的酸性的检验。
本研究结合以上文献的改进思路,采用定制的双边具支试管作为反应、性质检验以及净化装置;连接双联打气球和气球,使整个装置呈封闭状态;使用脱脂棉团检验二氧化硫的相关性质,试剂用量少;利用注射器向试管内加入蒸馏水对产物进行检验,现象明显。
3 浓硫酸与铜反应实验改进
3.1 实验用品
实验仪器:双边具支试管(三只)、酒精灯、双联打气球、硅胶塞、气球、镊子、注射器(带针头)、酒精灯、铁架台、胶头滴管、火柴、橡胶管、试管
实验药品:铜丝、浓硫酸(98%)、品红溶液、酸性高锰酸钾溶液、甲基橙溶液、蒸馏水、饱和氢氧化钠溶液、脱脂棉
3.2 实验步骤及现象
(1) 完整的实验装置如图2所示。连接好实验装置,然后检验装置的气密性。方法为:用双联打气球向装置内鼓气,若看到右侧气球膨胀,则说明气密性良好。
(2) 用胶头滴管吸取约2mL浓硫酸于试管1中。
(3) 取一根长约18cm铜丝将下端拧成螺旋状,上端涂抹一点凡士林然后穿过硅胶塞,将其放在试管1上,此时调节好铜丝的高度,避免铜丝和浓硫酸接触。
(4) 取三团脱脂棉,分别浸润品红溶液、甲基橙溶液、酸性高锰酸钾溶液,然后将其依次放入试管2中,最后在试管2的支管口处放一团干燥的脱脂棉[5]。
(5) 用饱和氢氧化钠溶液浸润三团脱脂棉,然后将其放入试管3的支管口处,最后在试管3的另一个支管口套上气球。
(6) 点燃酒精灯,对浓硫酸进行加热至产生大量酸雾,向下推动铜丝,让铜与浓硫酸接触反应。此时观察到铜丝和浓硫酸剧烈反应,试管1中产生浓雾,铜丝表面产生大量气泡,试管底部有灰白色固体生成。试管2中酸性高锰酸钾棉团的颜色逐渐退去,最后变成无色;甲基橙棉团的颜色由橙色变成红色,随着反应进行,红色慢慢变深;品红棉团的红色渐渐变浅,最后退至无色。气球有些膨胀。
(7) 抽离铜丝,停止加热,反应结束。用酒精灯对试管2的品红棉团慢慢加热,观察到试管底部内壁附着的试液又变成红色,试液表面上有气泡产生,棉团也逐渐变红,说明二氧化硫漂白品红的不稳定性。待试管2冷却后,观察到品红棉团又退至无色,说明二氧化硫漂白的可逆性。
(8) 用注射器向试管1中加入蒸馏水,静置,发现上层清液呈浅蓝色,上下抽拉铜丝对溶液进行搅拌,灰白色固体部分溶解,上层液体蓝色加深。
(9) 用双联打气球向装置内鼓气,确保装置内二氧化硫被试管3的氢氧化钠脱脂棉团完全吸收。挤压气球,处理来不及被氢氧化钠棉团吸收就逸出到气球里的二氧化硫。
3.3 关于该实验的几点说明
(1) 脱脂棉团浸润甲基橙等溶液不宜全浸透,可以借镊子将面向观察者这一侧的棉团润湿,另一半保持干松,以便于透气。试管3中的脱脂棉团可以稍稍浸透烧碱溶液,但也要保持透气。
(2) 实验开始前,铜丝和浓硫酸之间间隔一定的距离,否则铜丝与酸雾反应,表面会生成黑色物质。实验开始时,应将浓硫酸加热至表面有大量白雾时,才将铜丝伸入到浓硫酸中,减少副反应的发生。
(3) 实验前须用砂纸对铜丝进行打磨,不然可能会观察到溶液变成绿色,这是因为厂家常在铜丝表面加一层聚氯乙烯覆膜,导致反应混合物中含有Cl-,在反应体系中形成[CuCl4]2-,与水合铜离子混合呈现绿色[6]。
3.4 实验改进后的优点
(1) 用质地柔软且弹力较好的硅胶塞代替橡胶塞,气密性较好,在铜丝上涂抹凡士林,能够较好地抽拉铜丝控制反应的发生与停止。
(2) 增加了浸润饱和氢氧化钠溶液的棉团数量,能有效吸收多余的二氧化硫同时可以防止倒吸。用棉团分别浸润品红等溶液验证二氧化硫的性质,实验药品用量较少但现象却很明显。
(3) 使用双联打气球能够有效排尽装置内残留的SO2,避免污染空气。
(4) 在装置结尾处连接一个气球,通过气球的膨胀程度,可以实时监测装置的气密性。
(5) 利用注射器向试管1中添加蒸馏水,操作简单,不但可以看到溶液变成蓝色,搅拌之后还能观察到固体物质的溶解情况,从而判断白色固体是无水硫酸铜。
(6) 以甲基橙溶液作为指示剂,证明了二氧化硫溶液溶于水后呈酸性,还加强了学生对酸碱指示剂的认识。
参考文献:
[1]王晶,郑长龙主编.普通高中教科书·化学(必修)第二册[M].北京:人民教育出版社,2019:5.
[2]李文杰.浓硫酸与铜反应实验的改进[J].化学教学,2019,(7):63~65.
[3]魏崇启.浓硫酸与铜反应实验的创新改进[J].化学教学,2012,(9):47~49.
[4]张红卫.浓硫酸与铜反应实验的改进[J].化学教学,2020,(1):67~69.
[5]张苗,万鑫洁,彭新月.铜与浓硫酸反应装置的新设计[J].化学教学,2023,(11):65~68.
[6]王春.铜与浓硫酸反应实验异常现象的探究及装置的新设计[J].化学教学,2020,(11):76~79.