基于项目式学习的初中化学实验复习
作者: 李俊红
摘要: 从生活问题“每袋含钙500mg是真的吗”出发,确立“测定碳酸钙D3颗粒中的钙含量”为项目式学习主题,通过“实验探究: 测出碳酸钙D3颗粒和足量盐酸反应生成二氧化碳的质量或体积”“数据处理: 计算碳酸钙D3颗粒中的钙含量”“模型建构: 图示实验法进行科学探究的基本过程”等三个学习任务,融化学知识复习于真实问题解决的探究实践,有效提升了复习效果。
关键词: 钙含量测定; 项目式学习; 复习教学; 实验探究
文章编号: 1005 6629(2022)08 0060 07
中图分类号: G633.8
文献标识码: B
传统复习课教学往往以知识再现归纳、习题讲练促学为基本方式,不利于激发学生学习兴趣、培养学生解决真实问题的能力[1]。而项目式学习能够使学生经历成果导向下的综合任务完成过程,形成真实情境下的复杂问题解决思路,对培养学生的实践应用及迁移创新能力有独特的功能和价值[2]。“测定碳酸钙D3颗粒中的钙含量”项目式学习,从真实问题“每袋碳酸钙D3颗粒含钙500mg是真的吗”出发,让学生亲身经历确立项目主题、规划项目方案、实施项目方案和交流项目成果的全过程,“用中学”促进学生对实验室制取二氧化碳的原理、装置气密性检查、质量守恒定律以及根据化学式、化学方程式计算等化学核心知识技能的深刻理解,在探究实践中形成设计方案、进行实验、证据推理、反思评价等关键能力,感受化学从抽象的符号背诵到解决实际问题的“有用”和“有趣”。
1 项目主题和目标
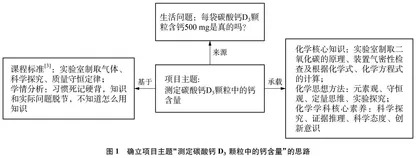
项目主题确立思路如图1所示。
项目学习目标如下:
(1) 根据补钙剂包装和使用说明书,计算补钙剂中含钙的质量和钙含量。
(2) 根据解决项目核心问题的实验原理,规划出解决定量实验问题的方案(质量法和体积法)。
(3) 基于实验目的评价: 选择实验装置,检查装置气密性,通过实验探究测出1袋碳酸钙D3颗粒与足量盐酸反应生成二氧化碳的质量或体积,在对比实验中发展收集证据、解释结论、反思评价、合作沟通、创新实践等关键能力。
(4) 根据实验数据算出碳酸钙D3颗粒中的钙含量,形成用反应中物质比例关系解决问题的定量思维。
(5) 评价结果的可靠性,培养审辩意识和科学态度,建构用实验探究解决化学问题的基本方法和思路。
2 项目学习流程
项目学习过程主要包括四个核心环节: 确立项目主题(抽提驱动性问题)→规划项目方案(梳理问题进阶和解决方案)→实施项目方案(实验探究和证据推理)→交流项目成果(成果展示和模型建构)。确立项目主题和规划项目方案为第1课时[对应学习目标(1)(2)],实施项目方案和交流项目成果为第2课时[对应学习目标(3)(4)(5)]。项目学习流程及课时分配如图2所示。
3 项目实施过程
以第2课时为例,呈现项目活动过程中的部分师生关键行为,从学生课堂表现、成果展示和后测分析,可看出活动实施的效果。
3.1 任务引入
[布置任务]上节课同学们规划了项目方案: 测出1袋碳酸钙D3颗粒中含碳酸钙的质量,算出1袋碳酸钙D3颗粒中含钙的质量以及钙含量;梳理出要解决的核心问题: 测出1袋碳酸钙D3颗粒中含碳酸钙的质量;厘清了实验原理: 测出碳酸钙和足量盐酸反应生成二氧化碳的质量或体积,根据化学方程式即可求出碳酸钙的质量及钙含量。本节课我们将通过实验探究的方法解决该问题,首先根据实验原理确定实验装置。下面展示几位同学用称质量(法)和量体积(法)设计的实验装置(见图3和图5),请谈谈设计意图,设计者的想法是否合理?如何改进?说明理由。
3.2 装置确定
3.2.1 质量法
[交流与讨论]
学生1: 用向上排空气法[见图3(a)]把二氧化碳收集到瓶内,盖好,用电子天平称重,扣除原集气瓶(含盖)的质量,即为生成二氧化碳的质量。
学生2: 这不是二氧化碳的质量,是二氧化碳和瓶内空气的质量差。除非收集气体前把瓶内抽成真空。
学生3: 抽成真空也不行,在收集过程中能保证空气不进入瓶内吗?还有,万一集气瓶规格小,不够收集气体,换瓶收集也会造成误差。这个方法不可行。
[评价与设问]考虑到集气瓶的规格问题,这是定量实验需要注意的。多数同学设计此方案,忽略了原集气瓶并不“空”,抽成真空的做法可操作性不强。用其他装置怎么测出二氧化碳的质量?
[交流与讨论]
学生1: 我模仿课本设计装置[见图3(b)],先称出反应前反应物和装置的总质量m1,把试管中的盐酸倒入烧杯内,等天平示数稳定,反应后剩余物和装置的总质量为m2,m1减m2即为生成二氧化碳的质量。
学生2和3: 我们设计的装置[见图3(c)(d)]和图3(b)的实验原理相同,优点是: 通过分液漏斗或注射器可以控制反应速率,同时避免试管底部粘上固体药品,倾倒盐酸时药品掉在外面,造成误差。
学生4: 我想用无水硫酸铜[见图3(e)]吸水,干燥二氧化碳,水蒸气不会跟着二氧化碳一起跑掉,数据更准确。
[评价与追问]利用质量守恒定律解决问题,设计巧妙。设计图3(e)的同学考虑到二氧化碳潮湿引起的误差,用干燥剂对装置作了改进,思维缜密。本节课老师提供的实验装置是图3(d)和(e),请推测改进后的实验数据是变大还是变小?需要检查装置气密性吗?如何检查?说明理由。
[交流与讨论]
学生1: 干燥剂吸水,相比不吸水,跑出去的更少了,所以改进后的数据比改进前应更小。
学生2: 不用查气密性,就是要让二氧化碳跑出去的。
学生3: 图3(d)不用查。图3(e)要查,因为要让生成的二氧化碳经过干燥剂,如果进干燥剂之前气体已经漏了,干燥剂没啥作用。
学生4: 可以把干燥管出口堵住,向下推压注射器活塞,若注射器活塞能复位,则气密性好。
学生5: 可以在干燥管出口接导管放入水中,加热锥形瓶,导管口有气泡,则气密性好。
[评价与设问]同学们分析得很到位,可见是否检查装置气密性,因实验目的而定,不能一概而论。除了实验室提供的装置,第5小组用两支注射器也能测出二氧化碳的质量,他们是怎么做到的?
小组5: 实验用药品是1袋碳酸钙D3颗粒(3g)和稀盐酸20mL,注射器可以从底部把残留气体顶出,减小误差。开始用两个30mL的注射器到实验室试做,发现盐酸容易喷出,然后把一个30mL的注射器换成100mL。实验步骤如图4所示。
[小结]根据质量守恒定律,利用气体的发生装置能测出生成二氧化碳的质量;实验数据并非越大越准确,视具体情况而定;实验装置除了实验室提供,也可以用生活替代品自制,装置需要在实践中不断完善和改进。
3.2.2 体积法
[交流与讨论]
学生1: 我设计的装置是图5(a)。在量筒的每一个大刻度处放一支燃着的小蜡烛,二氧化碳通入量筒内,二氧化碳密度大于空气,蜡烛熄灭时对应的刻度示数即为生成二氧化碳的体积。
学生2: 量筒那么窄,蜡烛怎么放进去。且量筒不能受热,可以用集气瓶。
学生3: 集气瓶也不行,因为蜡烛燃烧会生成二氧化碳,增加了变量。
[评价与设问]对,同学们分析得都有道理。再者,氧气浓度低于一定值,可燃物燃烧会停止,即蜡烛熄灭时对应的刻度也不一定是收集二氧化碳到达的高度。其他装置可以达成实验目的吗?
[交流与讨论]
学生1: 我想利用生成的二氧化碳往外推注射器活塞[见图5(b)],注射器前后刻度差即为二氧化碳的体积。
学生2: 不行,二氧化碳会从长颈漏斗跑走,应换成分液漏斗。还得预估一下生成二氧化碳的体积,准备足够容量的针筒。
学生3: 我利用二氧化碳产生的气压把水压入量筒[见图5(c)],量筒内水的体积即为二氧化碳的体积。
学生4: 不行,水根本压不过去,因为产生二氧化碳的导管口在液面下,一部分二氧化碳溶于水,溶不了的沿导管跑入量筒。须改进装置如图5(d)所示。
学生5: 水会吸收一部分二氧化碳,有误差,可以加一层植物油阻隔二氧化碳碰到水[见图5(e)]。
[评价与追问]很好。定量实验一定要有“量”的意识。本节课老师提供的实验装置是图5(d)和(e), 请推测装置改进后,测得二氧化碳的体积是增大还是减小?此实验成功的关键是什么?怎么操作?说明理由。
[交流与讨论]
学生1: 有油封的装置,二氧化碳碰不到水,水吸收不了二氧化碳,压进量筒的水应更多,即改进后比改进前数据更大。
学生2: 水要导流,装置必须不能漏气。
学生3: 可利用热胀冷缩原理,用热毛巾捂住锥形瓶,若水导流入量筒,则气密性良好。
学生4: 也可推压注射器活塞,若水导流,则气密性良好。
[评价与追问]推压注射器活塞,没有外加设备,操作更为简便。若提拉注射器活塞,预测有什么现象能证明装置气密性好?若注射器活塞从20mL处开始推压到底,即压缩空气20mL,则导流过来水的体积应是多少?本实验所用盐酸的体积是20mL,请问反应产生气体排出水的体积就是生成二氧化碳的体积吗?若不是,应作怎样的处理?
[演示实验]检查装置[图5(d)]的气密性。
[交流与讨论]
学生1: 提拉注射器活塞,相当于增大装置内气体体积,装置内气压减小, 大气压会把空气沿着量筒内的导管压入水中,水中导管口冒出气泡,说明气密性良好。
学生2: 实验观察导流到量筒内水的体积是13mL。
学生3: 生成二氧化碳的体积应是排出水的体积减去13mL。
学生4: 观察导管内水有残留,不能全部进入量筒。
[评价与设问] 对于比较复杂装置的气密性检查,一是不能改变装置,二是操作简便,三是现象明显,且和结论有逻辑关联。导管内残留水的体积加13mL约为20mL。这说明即使没有开始反应,挤压装置内多少体积的空气就会导流出多少体积的水,
所以生成二氧化碳的体积应是排出水的体积减去20mL。除了实验室提供的装置,第10小组还用两个矿泉水瓶和吸管等设计了测量生成二氧化碳体积的装置(见图6),请他们分享做法。
小组10: 改进前,把碳酸钙D3颗粒和盐酸依次加入瓶子,用
排水法收集二氧化碳,矿泉水瓶原体积减去瓶内剩下水的体积,即
二氧化碳的体积;改进后,盐酸改用注射器注入瓶内,我们想对比
改进前后二氧化碳体积的变化。
[小结]除了实验室提供的装置,利用注射器和矿泉水瓶等自主设计装置,经济环保也很有创意。装置确定好了,下面开始分组实验。
3.3 实验探究(测出1袋碳酸钙D3颗粒和足量盐酸反应生成二氧化碳的质量或体积)
[分组实验]全班53人,每5~6人一组共10个组,其中5个组做称质量(法),5个组做量体积(法)。每个组在组长负责下分成2个小组(同时完成改进前和改进后),数据本组共享。教师巡视指导。
[展示]小组实验数据见表1(由于数据较大,允许学生使用计算器)。
3.4 数据处理