浅析不同备考阶段框图推断题的复习策略
作者: 孙洁
摘 要:通过对2011~2021年的河北省中考化学框图推断题进行汇总分析,提出了在不同阶段针对框图推断题的复习策略与方法。即第一轮复习以章节为主线,通过梳理已有知识构建物质转化关系;第二轮复习以专题复习为主线,通过归纳常见的题眼和物质转化模型寻找解题突破口;而冲刺阶段则通过加强综合性训练,来提高学生综合运用知识解决问题的能力。
关键词:中考化学复习;框图推断题;教学策略
中图分类号:G633.8 文献标识码:A 文章编号:1009-010X(2022)14-0014-06
框图推断题是各地中考化学试卷中的常见题型,也是近几年河北省中考理综试卷的必考题型。框图推断题具有涉及知识范围广、思维容量大、综合性强等特点,既能考查学生对元素化合物知识的储备和掌握情况,又能检测学生对知识的综合运用能力以及证据推理能力。笔者通过对2011~2021年的河北省中考化学试卷中的框图推断题进行分析,探索出了不同备考阶段的框图推断题复习策略与方法。
一、梳理已有知识,构建转化关系
第一轮复习以章节为主线,注重单元内知识的联系,目的是夯实“双基”。在第一课时,教师可指导学生以某种或某类常见物质,如O2、CO2、H2O、金属或酸碱盐为核心构建物质转化关系图,并书写涉及的化学反应方程式,其中有核心物质参加的反应可以体现出该物质的化学性质,有核心物质生成的反应可以体现出其制法,如此有利于学生进一步熟悉已有知识,构建物质转化关系。为了防止知识点遗漏,在构建过程中,教师还可以引导学生用分类的思想对知识进行梳理。
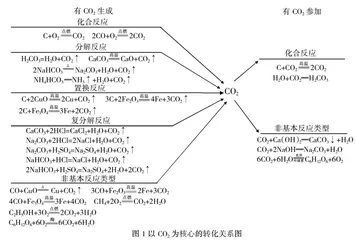
图1为学生构建的以CO2为核心的转化关系图,其从反应类型的角度入手进行了归纳,包括有CO2生成的化合反应、分解反应、置换反应、复分解反应及非基本反应类型的反应,以及有CO2参加的化合反应及非基本反应类型的反应,同时引导学生关注其中的相互转化关系。
图2归纳了能与CO2相互转化的五种物质,如单质为O2、氧化物为CO、酸为H2CO3、盐为CaCO3和Na2CO3.而这些物质间也存在一定的转化关系,如Na2CO3可以转化为CaCO3.
在此过程中找出常见单质、氧化物、酸、碱、盐之间的联系,然后由点连线,形成知识网。这些知识网其实就是框图推断题的原型,即将知识网进行简化,用字母替代物质,再给予一定的信息提示就是考试中见到的框图推断题了。图3为以CO2为核心的原创框图推断题,为强化学生对物质转化关系的理解,教师在第二课时时可利用该形式考查学生的知识建构水平。这一过程,既能丰富学生的知识储备,又能帮助学生形成研究物质性质及其相互转化关系的基本思路,如此可为框图推断题的复习奠定基础。
A~H是初中化学中的常见物质,它们的相互转化关系如图3所示,已知D是常见的温室气体,H常用作食品干燥剂,A、F属于单质,B、E属于盐,请写出下列反应的化学方程式。
1.写出反应①的化学方程式
若为化合反应,则该反应的化学方程式为:
__________________________________________
若为置换反应,则该反应的化学方程式为:
_________________________________________
2.写出反应②的化学方程式
若为化合反应,则该反应的化学方程式为:
________________________________________
若为非基本反应类型,且用于工业生产,则该反应的化学方程式为:
3.写出反应③的化学方程式:
___________________________________
4.写出反应④的化学方程式(非基本反应类型): _________________________
5.写出反应⑤的化学方程式:
____________________________________
6.写出反应⑥的化学方程式:
______________________________
7.写出反应⑦的化学方程式
若为分解反应,则该反应的化学方程式为:
__________________________________
若为复分解反应,则该反应的化学方程式为:
8.写出反应⑧的化学方程式
若为复分解反应,则该反应的化学方程式为: ________________________________
若为非基本反应类型,则该反应的化学方程式为:_________________________________
9.写出反应⑨的化学方程式:
____________________________________
10.写出反应⑩的化学方程式:
______________________________________
二、深挖题目信息,寻找解题突破口
第二轮复习以框图推断题的专题复习为主线,意在提高学生对单元间知识的把握能力和对知识的应用能力,以便构建出更加全面的知识网络和体系。图4为学生构建的初中化学常见物质的转化关系图。
-此时学生已经具有了一定的知识储备,但由于框图推断题的综合性强、信息隐蔽,所以学生找不到解题的突破口,解题时也费时费力。因此在进行第二轮框图推断题的复习时,笔者以《义务教育化学课程标准(2011年版)》为依据,以教材为载体,对2011~2021年的河北省中考化学框图推断题进行了汇总分析,并对经常考查的物质进行了统计(见表1),其中对H2、Fe、Cu、Fe2O3、CO2、CO、H2O和Ca(OH)2的考查最为频繁,考查角度往往是从物质的类别、颜色、用途、组成等入手。
教师指导学生总结H2、Fe、Cu、Fe2O3、CO2、CO、H2O和Ca(OH)2的用途,并从物质的类别、颜色、组成等角度对其进行归纳。这意在让学生熟悉常考的热点,以便顺利找到解题的突破口,也就是常说的题眼。除了物质的类别、颜色、用途和组成外,常见的题眼类型还包括物质的特殊性质、特殊反应现象、物质的俗称、物质之最、元素之最等,也可让学生从上述角度入手对初中化学中的常见物质进行归纳总结。
图5的框图推断题,可以从以下几个角度命题:
1.A为暗紫色固体,甲、乙、丙、H为黑色固体,K为常见的白色沉淀,Q为红色固体,P为浅绿色溶液(题眼为物质的颜色)。
2.E可以供给呼吸,F可以用于灭火,H为磁铁矿的主要成分,I为常见的食品干燥剂,L为最清洁的能源,丙为日常生活中用途最广泛的金属(题眼为物质的用途)。
3.E能使带火星的木条复燃,F能使澄清的石灰水变浑浊,①反应剧烈燃烧、火星四射,②反应有红色物质析出(题眼为反应的现象)。
4.B和D、F和G的组成元素相同,且F、G为气体,H为磁铁矿的主要成分,L为非金属单质,Q为常见的金属单质(题眼为物质的分类、组成)。
参考答案:A为KMnO4,B为H2O2,C为K2MnO4,D为H2O,E为O2,F为CO2,G为CO,H为Fe3O4,I为CaO,J为Ca(OH)2,K为CaCO3,L为H2,M为H2SO4,N为CuSO4,P为FeSO4,Q为Cu,甲为MnO2,乙为C,丙为Fe.
同样的框图,配以不同的题干,分别从物质的颜色、物质的用途、反应现象、物质的分类和组成角度入手,均可推断出同样的答案。题眼是解决框图推断题的关键,学生不仅要知道题眼,还要做到会用题眼。为了巩固学生的学习成果,教师可采用课堂小测的形式对学生进行考查,即给出反应现象、用途、物质的俗名、条件等,要求学生写出对应的化学反应方程式。
方式一,反应现象和反应类型相结合,写出所涉及反应的化学方程式:溶液由无色变成蓝色的置换反应;溶液由无色变成蓝色的复分解反应;有蓝色沉淀生成的复分解反应;黑(红棕)色粉末变红(黑)的置换反应;黑(红棕)色粉末变红(黑)的非基本反应类型的反应;有白色沉淀产生的复分解反应;有白色沉淀产生的非基本反应类型的反应等。
方式二,用途和俗名相结合,写出所涉及反应的化学方程式:熟石灰改良酸性土壤的反应;小苏打治疗胃酸过多;纯碱溶液与澄清石灰水制烧碱的反应;生石灰作干燥剂等。
方式三,反应类型与条件、能量变化相结合,写出所涉及反应的化学方程式:常温下大量放热的化合反应;常温下大量放热的置换反应;常温下发生放热但现象不明显的复分解反应;点燃时放出大量热的非基本反应类型的反应等。
在分析框图推断题时,不仅要找到题干中的题眼,还要挖掘出框图中隐含的典型物质相互转化的信息。例如在题干中只提到反应条件略去,生成物、反应物未略去的情况下,我们可以关注物质的转化模型,即引导学生利用框图分析反应类型,并归纳初中化学中涉及的“一变二”“一变三”“二变一”“二变二”“二变三”反应的化学方程式。
例1.(2018年石家庄市桥西区一模)甲、乙、丙、丁、戊都是初中化学常见的物质,请回答下列问题。
(1)如图6所示是甲、乙、丙、丁的转化关系(反应条件已略去)。
①若甲、乙、丙都是化合物,丁是单质,则丙的化学式为______________,写出丙的一种用途_________________。
②若甲、乙都是黑色粉末,且该反应为置换反应,则该反应的化学方程式为 __________________
_________________(写出一个即可)。
③若该反应在溶液中进行,甲、乙、丙、丁都是化合物,其丁为水,则该反应可能是中和反应,还可能是______________(填物质的类别)和酸的反应。
(2)如图7所示是甲、乙、丙、丁、戊的转化关系(部分生成物已略去)。若五种物质都是化合物,其中丙为白色沉淀,戊为无色无味的气体,且所有反应都在溶液中进行。则甲和乙反应的化学方程式为 ______________________。上述五种物质中能使无色酚酞溶液变红的有
_____________________填化学式)。
试题分析:该题属于“一图多解”,即题目设置了不同的推断要求。(1)中明确说明反应条件已略去,所以图6为“二变二”的反应,可能是基本反应类型中的置换反应、复分解反应,也可能是非基本反应类型的反应。①若甲、乙、丙都是化合物,丁是单质,则该反应不属于置换反应或复分解反应,而应为一氧化碳与金属氧化物的反应,生成的是二氧化碳和相应的金属单质,故丙是二氧化碳,其能用于灭火。②若该反应为置换反应,则其可能为活泼金属与酸、金属与盐溶液、碳或氢气与金属氧化物的反应,由于甲、乙都是黑色粉末,所以该反应是碳与氧化铜(或四氧化三铁)的反应,生成的是二氧化碳和铜(或铁)。③若该反应在溶液中进行,甲、乙、丙、丁都是化合物,其丁为水,则该反应可能是中和反应,还可能是金属氧化物和酸的反应。(2)中明确说明部分生成物已略去,所以图7为“二变二”或“二变三”的反应,五种物质都是化合物,所以不可能是置换反应,其中丙为白色沉淀,戊为无色无味的气体,且所有反应都在溶液中进行,所以该反应有可能是氢氧化钙与二氧化碳的反应,生成的丙是碳酸钙,戊是二氧化碳,甲是氢氧化钙,乙是碳酸钠,生成的丁是氢氧化钠,因此甲和乙反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,上述五种物质中能使无色酚酞溶液变红的有氢氧化钙、碳酸钠和氢氧化钠。