中考化学热点题、易错题解法探究
作者: 李凤清【摘要】纵观全国各省、市中考试题,往往都能发现有关金属活动性顺序内容的试题,这也是中考命题的核心考点之一。笔者将与金属活动顺序有关的题目归结为“热点题”和“易错题”,文章对这两类题目出错的原因进行探析,并指出易错的原因,然后对解决题目所需知识点进行系统归纳与总结,使其降低解题难度。同时,教师应根据教学需要,尽可能尝试各种不同的解法,以此来帮助学生选用适合自己的解题方案,从而提高学生核心素养。
【关键词】中考;化学;热点题;易错题;解析
【中图分类号】G633.8【文献标志码】A【文章编号】1004—0463(2023)19—0123—05
纵观近几年全国各个省、市中考试题,在初中化学命题中,不难发现以有关金属活动性顺序内容为考查对象的试题,这类试题几乎每年各省必考。考查的方式很多,笔者认为常见的题型有两类:一是“利用一种或多种金属与盐溶液发生置换反应的结果与现象来推断滤液、滤渣的成分”为题材设计的题目,即“热点题”;二是“利用活泼金属与某些稀酸反应放出氢气的质量及所需的反应时间之间的关系用图表的形式展现出来,进而要求学生从图表中提取相关信息来推断参加反应的金属的活动性顺序及参加反应、且没有可变化合价金属质荷比,或者有可变化合价金属的最大质荷比的大小(活泼金属有可变化合价时,与稀酸反应放出H2的反应中显示最低价态,所以此时该金属的质荷比最大)”为题材设计的题目,即“易错题”。这两类题目在考试中,学生的得分率往往不高,失分现象很明显,究其原因时不难发现:热点题往往因题中提供的信息量多,且这些信息之间往往错综复杂,学生无法从中筛选出重点信息,给学生答题带来了阻碍与干扰,致使许多学生无法结合题目内容理顺各信息之间的关系,再加上学生本身缺乏科学推理的能力,引起学生思维混乱,无法进行有效推理,得不出正确的结论。而易错题因学生无法结合图表提取有关图表中的各种信息,难以完成数与形的有机结合,再加上平时教学中没有及时总结出规律供学生强化使用,导致学生容易出错。
下面就这两类题型的解法进行探究,以帮助学生提升应试技能与技巧,减少应试失分,引导学生积累解题经验,从而提升解决问题的能力。
一、热点题解法探究
热点题解题的关键在于帮助学生理顺思维,让其掌握解题技巧。在教学中指导学生按下列步骤解题,并结合题意完成分析、推理,避免遗漏有关信息。在解决这类问题时,应分上、下两部分,人为规定:上部分为滤渣层,下部分为滤液层。在上部分滤渣中,应结合题目中提供的各种信息把涉及到的所有金属对应的化学式写出来,并按照金属活动性由强到弱的顺序写出,书写时一定注意,金属活动性越活泼越往前排列,越不活泼越往后排列;对于下部分滤液,在上部分已写出金属单质化学式的正下方对应位置上,分别写出各种金属参加反应时所显示的对应金属离子符号,不需写出化合物中的阴离子符号(因为金属与盐溶液发生置换反应时,其置换反应发生在金属与盐溶液中的阳离子之间,而阴离子之间不发生置换反应,因此阴离子不需写出);接着针对题中提供的信息,并结合以下五条法则进行分析推理,从而判断出滤渣中金属有无及滤液中金属离子的存在与否。
判断时,应遵循以下五条法则:
一是若题目中提及到的或者根据题意推导出某种活泼金属存在于滤渣中,则滤渣中肯定存在着不活泼金属,同时活泼金属也可能存在于滤渣之中;
二是若判断出或推导出盐溶液中有参加反应的较活泼金属离子存在时,则滤液中肯定存在与盐溶液参加反应的金属中更活泼金属以离子形式存在,但也可能存在与盐溶液参加反应的金属中的较不活泼金属以离子形式存在,这要根据题意进一步推理确定;
三是若参加反应的某种金属在滤渣中不存在时,则滤液肯定有该金属离子;若滤液中不存在参加反应的某种金属离子时,则该金属定在滤渣中存在;
四是若有大量H+存在溶液中,则固体中一定不存在活动性在H前的金属,反之,溶液中无H+,则固体中一定或可能存在活动性在H前的金属;
五是当多种金属与某种盐溶液发生置换反应时,具有顺序性。若参加反应金属中的最不活泼金属存在于固体滤渣中,而参加反应的金属中较不活泼的金属可能存在,也可能不存在于滤渣中,这与参加反应物量的多少有关,当然最活泼金属离子也一定在溶液中大量存在[1]。
判断时,为了方便操作,会引入一些特殊的符号表示特定的意义。通常用“√”表示全部有,“×”表示完全没有,“?”表示无法确定某种离子或物质有还是没有,“★”表示有但是无法确定是完全有还是部分有。最后让学生观察滤液、滤渣部分可综合得出结论。
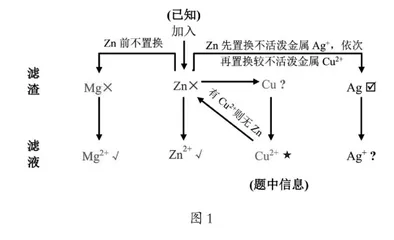
例如:某同学在探究置换反应条件时,把事先准备好的锌粉和铜粉按比例混合成的粉末加入到制备好的硝酸银和硝酸镁混合液中,待充分振荡后,再静置出现分层,经过滤得到不溶物滤渣及蓝色透明滤液。关于该固体和液体的组成成分说法正确的是()
A.把稀HCI滴加到滤渣中,充分振荡,结果可能产生气泡
B.滤液中一定有Cu(NO3)2、Mg(NO3)2和Zn(NO3)2
C.Ag定在滤渣中存在,Cu和Zn可能也存在滤渣中
D.AgNO3一定在滤液中不存在,Zn(NO3)2可能存在滤液中
解析:推理过程如图1。
某种盐溶液能否与加入这种盐溶液的多种金属之间发生置换反应,完全是由该种金属的活动性与参加反应盐溶液中的阳离子所对应金属活动性的大小决定的,不是随意可以发生的。当盐溶液中的金属离子对应的金属活动性若排在题目中涉及到的所有金属的最前面,则一定不能参与置换反应;若盐溶液中的金属离子所对应的金属活动性排在题目中涉及到的所有金属的最后面或中间时,则一定能跟所有金属或部分金属参与置换反应[2]。但置换也有顺序,首先是题目中所涉及到最不活泼的金属对应的离子Ag+优先被活泼金属Zn置换出来,待Ag+完全置换出来后,如金属Zn有剩余时,剩余金属Zn再去置换较不活泼金属对应的Cu2+离子,如金属Zn没有剩余时,溶液中的Cu2+全部存在溶液中,这样依次置换下去。因此,观察图1,从上层符号可以看出:金属Ag一定存在,金属Cu可能存在,肯定没有Mg和Zn;而在下层滤液中,一定存在三种离子,即Mg2+、Zn2+、Cu2+,而Ag+存在与否,题目中所提供的条件不足,无法作出有无的判断。故选B。
二、易错题解法探究
易错题易错的原因在于学生对图表所提供的信息不明确,对图像中各线段所表示的意义不能准确把握,难以与题目中提供的信息完成数与形的有机结合,因此教师必须要帮助学生识图是解决这类问题的关键,让学生明确图像中各线所表示的意义,使图像中提供的信息与题目中的信息有机结合,这样可为学生明确解题的思路与方法提供理论依据。图2是给大家提供等质量的活泼金属Mg、Fe、Zn分别与足量的某些稀酸反应放出H2的质量与参加反应所需时间之间关系的示意图。
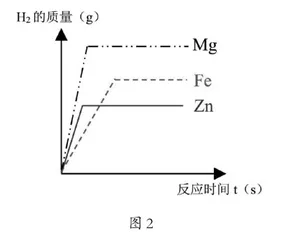
从图2中可以看出,因金属的活泼性不同,它们与足量的稀酸反应放出H2的速率不同,同时因不同活泼金属的活泼性不同,导致三种质量相等的不同金属与足量的稀酸反应产生的H2的质量也不同。图中3条斜线的斜率大小不同,其斜率的大小取决于金属活动性的大小,它们金属活动性的大小决定着金属与稀酸反应放出H2的快慢。各种不同活泼金属的活泼性及其与稀酸反应速率的快慢可利用图像中初始线段的斜率大小去判断,活泼金属的活泼性及其与稀酸反应速率跟图中斜线的斜率成正相关系,即斜率大的金属活动性肯定大于斜率小的金属活动性,且斜率大小与金属活动性大小成正比关系,因此斜率越大的代表着对应的金属活动性就越大,与某些稀酸反应时生成H2速率就越大,反之相反[3]。而水平线的高低代表着等质量金属与足量的稀酸发生完全反应时产生H2量的多少,并且水平线越高,代表等质量该种活泼金属与足量的非氧化性稀酸充分反应放出H2量就越多,相反,该金属原子的相对质量与参加反应时所带电荷之比(即质荷比)肯定越小,因为Mg、Zn、Fe与稀酸反应放出H2时都显+2价,因此质荷比小的这种金属的相对原子质量就必然越小,反之则相反。
另外,当多条水平线完全重合为一线时,表明此时产生H2的量相同,说明参加反应的稀酸已经用完,没有剩余,至少质荷比小的金属有剩余,金属原子的质荷比越小,剩余的可能性就越大[4]。这些结论是解决这类题目的理论依据,在平时的教学中应给学生归纳总结,以便遇到这类题目时使用。
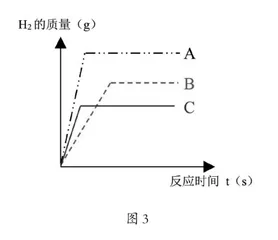
例如:为了研究不同金属之间活动性差异,某同学选用A、B、C三种活泼性不同的金属,分别称取等质量的三种金属投入足量的稀H2SO4溶液完全反应(假设三种金属均不与水反应,但都与稀硫酸能反应,且形成化合物时均显+2价),并把这三种金属与足量的稀H2SO4溶液生成H2的量(g)与参加反应时间t(s)之间的关系绘制成图3。
观察分析图像后,得出了一些结论,你认为不合理的是()。
A.三种金属参加反应时的速率不同,依次为:A > B > C
B.三种金属在反应中显示不同活动性,依次为:A > C > B
C.三种金属与足量的非氧化性稀酸反应生成H2的量也不同,由多到少依次为:A、B、C
D.如三水平线重合时,稀硫酸反应完全,至少活泼金属A、C有剩余
解析:不同活泼金属与足量的稀酸溶液反应速率大小、金属活动性的强弱与图像中斜线的斜率大小成正相关系。从图像来看,因参加反应的金属A所对应斜线的斜率最大,而金属B所对应斜线的斜率最小,因此三种金属分别与足量的稀硫酸反应的速率由快到慢依次为:A、C、B;从三条斜线的斜率大小来看,三种金属分别与稀H2SO4显示出的活泼性也不同,由强到弱依次应为A、C、B;由三条水平线的高低决定生成H2的量的多少,反应完全后,生成H2的量由多到少依次应为:A、B、C;当三条水平线重合时,说明稀硫酸溶液反应完全无剩余,至少相对原子质量较小的(即质荷比较小)金属A、C有剩余,故选A。
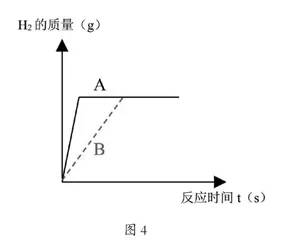
又比如,某化学兴趣小组的同学发现,不同的活泼金属材料与某种稀酸反应产生H2的质量和反应的速率都不同。但有的同学认为,这与金属的活动性大小有关。为了验证这一结论,便设计了以下实验。选用活泼性不同的两种活泼金属材料A、B,秤取质量相等A和B两种金属分别投入等质量等浓度的稀H2SO4溶液中,现将反应过程中产生H2的质量(g)与反应时间t(s)之间对应的数量关系绘图(如图4),你认为其中不正确的结论是()。
A.金属A与稀H2SO4液反应的速率快于金属B与稀H2SO4液反应的速率
B.最终生成的H2的质量相等
C.金属B与稀H2SO4反应显示的活动性强于金属A与稀H2SO4反应显示的活动性
D.若金属A、B中至少有一种剩余,而参加反应稀H2SO4没有剩余,完全参加了反应
解析:活泼金属与足量稀酸溶液反应速率快慢、金属活动性的强弱与图像中斜线的斜率大小成正比关系,从图中观察可以看出:金属A参加反应时的斜率较大,金属B参加反应时的斜率较小,这样金属A与稀H2SO4反应的速率大,金属A参加反应时显示出的活泼性肯定比金属B显示出的强些,而金属B正好相反。由于图4中的两条水平线完全重合,则说明稀H2SO4完全与两种等质量的金属A、B发生反应,最后生成的H2的量却相等,在这两个反应中,稀硫酸完全参加反应,肯定无剩余,但是两种不同种类的金属A、B,其相对原子质量肯定不同,在这两种金属A和B中,其中至少质荷比较小的金属在该反应中肯定有剩余,而质荷比较大的金属是否完全反应却无法确定,故符合题意的是C。
总之,在实际教学中,作为教师应该树立问题意识,遇到问题时应帮助学生边探究边归纳边总结,这样可对知识体系进行有效优化和构建,让学生在学会解决问题方法的同时,积累解决问题的经验与策略,真正实现“教而不教”的目的,为后续学习奠定基础,激发学习兴趣,而学生的综合技能随着问题的解决在不断提升与发展,往往可以使待解决的问题由难转易,这种有效的教学方式进而提高了教学的有效性。
参考文献
[1]张忠城.浅谈“金属单质与混合盐溶液反应”的解题策略[J].数理化解题研究,2018(29):89-90.
[2]张慧莹,杨永赏.河南中考“金属的性质”专题常见考点及例析[J].招生考试之友,2016(10):46-47.
[3]徐宜秋.初中化学金属与稀酸反应图像问题探究[J].数理化学习(初中版),2013(08):44-45.
[4]王锦科,张兆宽.金属与酸的置换反应中考题型解析[J].河北理科教学研究,2003(03):68-69+72.
编辑:张昀