活塞可固定式注射器的制作及实验改进
作者: 马力
摘 要: 制作并基于活塞可固定式注射器,将压强对气体溶解度的影响实验、不同压强下氧气溶解度测定实验、压强对化学平衡的影响实验、压强对化学反应速率影响的实验以及利用压强变化触发反应的硫酸亚铁与氢氧化亚铁制备的一体化实验进行了改进。改进后的实验操作简便、现象清晰,取得良好效果,新装置不仅适用于教师演示实验,也适合学生探究实验。
关键词: 活塞可固定式注射器; 压强影响; 实验改进
文章编号: 10056629(2024)10006805
中图分类号: G633.8
文献标识码: B
1 问题的提出
压强是表示压力作用效果的重要物理量,在中学化学的教学过程中则不仅需要利用压强变化检验装置气密性,还需要探究压强等因素对物质溶解度、化学平衡、化学反应速率等的影响。在教学实践中,受实验时间、实验仪器配备等多方面因素的影响,压强条件的定量控制并不易实现,这也在一定程度上影响了不同压强条件下的相关探究实验的开展,不利于学生系统建构相关知识的结构体系。能否通过一套相对简单的实验装置实现相对准确的压强控制,让学生能够拥有更多的机会实现自己动手探究?由此,本文设计制作了一套活塞可固定式注射器,并利用活塞可固定式注射器尝试对部分中学化学所涉及的压强相关实验进行了改进。
2 仪器的制作
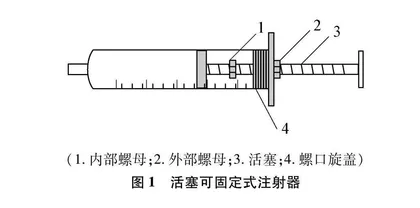
设计制作的活塞可固定式注射器如图1所示,活塞上安装有两个固定螺母(一个固定螺母在注射器主体内部,另一个固定螺母则在注射器主体外部),用于固定注射器活塞。注射器主体上设有螺口旋盖,如需调节注射器主体内部螺母,则可通过旋开螺口旋盖后调节[1]。实验时,将活塞可固定式注射器密封后,通过推拉注射器活塞改变气体体积从而实现内部压强的变化,而活塞用固定螺母固定后,则可使内部压强保持稳定。
3 实验设计与现象
3.1 压强对气体溶解度的影响
教材中并没有设计压强对气体溶解度影响的相关实验,在教学过程中教师往往是通过单纯的理论描述或是借助碳酸饮料开盖后产生气泡的现象进行介绍。但由于纯理论的描述相对枯燥,学生往往难以快速将其内化,而对于碳酸饮料开盖的现象,虽然较为常见且直观,但其实大部分学生并不熟悉碳酸饮料开盖前后压强所发生的变化,还需教师进行补充说明。基于以上存在的问题,笔者借助活塞可固定式注射器(以下简称注射器)将压强对气体溶解度影响的实验进行了如下设计。
3.1.1 实验装置
新设计的实验装置如图2所示。
3.1.2 实验操作步骤
(1) 使用活塞可固定式注射器(100mL)抽取10mL碳酸饮料(以常温常压下不再产生气泡为宜),然后用硅胶管将注射器口与压强传感器相连接。
(2) 将注射器倒置(注射器口朝上),快速抽拉注射器活塞至50mL刻度处,并旋动注射器外固定螺母将活塞固定。
(3) 调整(旋动)注射器外固定螺母,使活塞缓缓回升。
3.1.3 实验现象及实验数据
快速抽拉注射器活塞至50mL刻度处并固定后,可观察到碳酸饮料中产生大量气泡,压强传感器显示压强读数由101.1kPa先快速减小至6.8kPa,后逐渐回升。
调整(旋动)固定螺母使活塞回升,则可观察到碳酸饮料中气泡逐渐减少,压强传感器显示压强读数逐渐回升。实验中亦可使用自来水等替代碳酸饮料,观察到的实验现象基本一致,快速抽拉注射器活塞至50mL刻度处并固定后,自来水中也产生明显气泡,但数量略少,气压回升速度也较慢。
3.1.4 实验优点
运用活塞可固定式注射器可以较稳定地控制压强变化,实验现象明显,学生可以轻松得出压强对气体溶解度影响的结论,而且实验操作比较简单,学生可独立完成操作,也可安排用于学生探究实验。
3.2 不同压强下氧气溶解度的测定
日常教学过程中,由于压强等条件不易控制,实验装置复杂等问题,不同压强下气体溶解度的测定实验在中学阶段少有涉及。基于此,尝试使用活塞可固定式注射器(100mL)、溶解氧传感器、压强传感器、具支试管(大号)、胶塞、三通阀等组合装置,进行了不同压强下氧气溶解度的简单测定。
3.2.1 实验装置
新设计的实验装置如图3所示。
3.2.2 实验操作步骤
(1) 在具支试管中加入已通入氧气一段时间后的蒸馏水约25mL,将胶塞、溶解氧传感器与具支试管上口相连接,再将三通阀一端通过硅胶管与具支试管支管相连,然后将压强传感器、活塞可固定式注射器(100mL)分别与三通阀另外两端相连接。
(2) 打开三通阀,可通过抽拉注射器活塞减小具支试管内部压强,并用活塞外部固定螺母固定,待压强传感器、溶解氧传感器数据稳定后读取并记录数据。实验中可通过抽拉注射器活塞至不同位置,调节不同气压。
(3) 若要测量更大压强下氧气的溶解度,则可以通过注射器加入氧气以增大具支试管内部的压强,并通过旋开注射器的螺口旋盖,调节内部螺母的位置将活塞固定,然后再旋紧注射器的螺口旋盖,同样待压强传感器、氧气传感器数据稳定后读取并记录数据。实验中可通过加入氧气体积的不同,控制不同的气压增幅。
3.2.3 实验现象及实验数据
当抽拉活塞减小压强时,可观察到气泡冒出,溶解氧数据变小,当加入氧气增大压强时,则可观察到溶解氧数据变大,读取记录压强传感器、溶解氧传感器的多组实验数据,即可完成溶解度曲线的绘制。
3.2.4 实验优点
本实验操作简单,学生可以较方便地获得压强与溶解氧数据,从而绘制溶解度曲线,帮助学生建构压强与气体溶解度变化的关系模型。
3.3 压强对化学平衡状态的影响
在教学实践中,学生往往很难仅凭肉眼清晰观察到实验中压强对化学平衡移动时气体的颜色变化,虽然借助色度传感器能观察到迅速加压后,吸光度数据先迅速增大,后变小,最终数据比原数据大,但实验中快速推动注射器活塞会压缩气体做功产生热量,快速抽拉注射器活塞则反之,均会造成温度的影响,而且经计算该反应在压强改变后达到新平衡的时间为微秒级,难以很好地说明混合气体颜色变化就完全是因为压强改变所导致[2]。基于以上问题,借助活塞可固定式注射器、色度传感器等设计如下压强对化学平衡影响的实验。
3.3.1 实验装置
实验装置如图4所示。
3.3.2 实验操作步骤
(1) 在比色皿(45mm×12.5mm×12.5mm,容量3.5mL)中充满二氧化氮和四氧化二氮的混合气体,通过胶塞将比色皿与活塞可固定式注射器(10mL)相连接。由于此时色度传感器外盖无法完全关闭,故可用黑布盖住色度传感器表面,防止数值受外部环境影响。
(2) 实验开始前,先读取并记录色度传感器的初始数据,然后抽拉注射器活塞至3.5mL刻度处,并用注射器外部固定螺母将活塞固定。此处需要注意的是:由于快速抽拉注射器活塞会对气体做功,在一定程度上导致注射器内部温度发生变化,故可缓慢拉动注射器活塞,并需待吸光度数值保持稳定后再读取记录数据。
(3) 将实际吸光度数据与不考虑平衡移动时的吸光度数据相比较,即可判断出压强对化学平衡移动的影响。实验中亦可通过推动注射器活塞至目标刻度,并通过旋开注射器的螺口旋盖后,调节内部螺母的位置将活塞固定,然后再旋紧注射器的螺口旋盖,同样待吸光度读数稳定后再读取最终数据并与不考虑平衡移动的理论数据作比较得出结论。
3.3.3 实验现象及实验数据
色度传感器的初始数据吸光度为0.36AU,抽拉注射器至3.5mL刻度处(即体积增大一倍)测得平衡后的吸光度为0.28AU,根据比尔朗伯定律,与不考虑平衡移动时的吸光度数据0.18AU相比较,即可判断出压强对化学平衡移动的影响。
3.3.4 实验优点
本实验装置可以较为精准地改变气体的体积从而控制压强的变化,而通过将实验最终所得色度数据与不考虑平衡移动时计算得出的色度数据相比较,则可避免温度等因素的干扰,成功得出压强对化学平衡状态影响的相关结论。
3.4 压强对化学反应速率的影响
不少同行已对该实验进行了设计,取得了一定的教学效果,但仍然存在一些问题。例如设计选用线香燃烧反应,却存在学生并不了解线香的化学组成,且氧气浓度不易控制,使实验的成功率不高;设计选用二氧化碳与水反应、二氧化硫与氢氧化钠溶液反应等,却又存在气体溶解、平衡移动等多方面因素共同影响的问题;设计选用各类传感器,又存在实验操作复杂,实验耗时较长,实验现象不够直观等问题[3]。基于此,尝试使用活塞可固定式注射器(100mL)、二通阀等仪器,设计选用学生较为熟悉的硫化氢气体与二氧化硫气体常温下反应相关压强对反应速率影响的实验。
3.4.1 实验装置
实验装置如图5所示。
3.4.2 实验操作步骤
(1) 在同等压强条件下,用一支活塞可固定式注射器(100mL)收集20mL硫化氢气体后再抽入30mL空气,另一支活塞可固定式注射器收集10mL二氧化硫气体,将两支注射器通过二通阀相连接(在实验开始前使二通阀处于关闭状态),记为A组。
(2) 取两支活塞可固定式注射器分别在同等压强条件下收集20mL硫化氢气体、10mL二氧化硫气体,用于对照实验(实验开始前二通阀处于关闭状态),记为B组。将A、 B两组收集有10mL二氧化硫气体的注射器的内部螺母均固定于30mL刻度处。
(3) 同时打开A、 B两组的二通阀,推动收集有硫化氢气体的注射器活塞,迅速将其中气体全部推入收集有二氧化硫气体的注射器后,关闭二通阀。由于收集有二氧化硫气体的注射器在实验前已调节过活塞内部螺母,故活塞仅能被推动至30mL刻度处,而A组注入的气体中除了等量的硫化氢外还有空气,故压强相对较大。
(4) 快速调节两组收集有二氧化硫注射器的外部螺母,将活塞完全固定,防止气体相互反应后造成注射器活塞回落。
3.4.3 实验现象及实验数据
在实验中可清晰地观察到A组收集有二氧化硫气体的注射器壁上约8s后产生淡黄色固体,B组注射器壁上虽然在约20s后也逐渐产生淡黄色固体,但相对A组而言明显较慢。
3.4.4 实验优点
本实验现象直观、明显,实验用时较短,完全可以让学生自己动手在课堂中去探索。
3.5 利用压强变化触发反应的硫酸亚铁与氢氧化亚铁制备的一体化实验设计
一体化实验往往具备实验步骤连贯、实验耗时相对较短等优点,但也存在所用仪器较多,装置搭建较复杂,不便于课堂教学推广等问题。为此,尝试使用活塞可固定式注射器(100mL)、单向阀等仪器,利用压强变化触发化学反应进行硫酸亚铁与氢氧化亚铁的制备一体化实验设计。
3.5.1 实验装置
实验装置如图6所示。
3.5.2 实验操作步骤
(1) 取一支活塞可固定式注射器(100mL)打开螺口旋盖,抽出活塞后,加入10g铁片(过量)后装好活塞,调节注射器内部固定螺母于40mL刻度处,旋上螺口旋盖,推动活塞排出注射器内部空气后,将注射器与三通阀上端相连。
(2) 另取一支普通注射器吸取10mL 3mol/L稀硫酸,连接向外开启的单向阀后,再将单向阀与三通阀的下端相连。
(3) 再取一支普通注射器吸取煮沸后的15mL 6mol/L氢氧化钠溶液,连接向内开启的单向阀后,再将单向阀与三通阀右端相连。
(4) 抽拉装有铁片的注射器活塞,使装有稀硫酸注射器中的稀硫酸全部进入活塞可固定式注射器。
3.5.3 实验现象及实验数据
可以观察到铁片与稀硫酸反应迅速产生气泡,气体推动注射器活塞至40mL刻度处,由于螺母固定,故此时活塞不再移动,注射器中反应后的溶液被气体排出注射器,进入装有氢氧化钠溶液的注射器,并生成白色沉淀氢氧化亚铁,由于实验装置密闭,可以保存白色沉淀较长时间不变色。
3.5.4 实验优点
利用压强变化触发化学反应,实验操作难度低,实验耗时短,实验现象清晰可见,氢氧化亚铁白色沉淀保存时间长,有助于激发学生的学习兴趣和对反应原理的理解。
4 结语
基于活塞可固定式注射器对部分中学化学所涉及的压强相关实验进行了设计与改进,取得了良好的效果。在教学实践中,还可以引导学生思考实验装置原理、实验的本质,引导学生完成实验装置的再改进的探索,培养学生的创新意识。
参考文献:
[1]赵雯, 马力. 化学气体实验一体化装置的新改进[J].化学教学, 2022, (5): 72~74.
[2]王磊, 信欣, 孙影. 压强对化学平衡影响的再探究[J]. 化学教与学, 2023, (14): 86~91.
[3]顾仲良, 周学工. 压强对反应速率的影响实验探索——应用溴百里香酚蓝的色变[J]. 化学教与学, 2020, (4): 93~95.