铜与硝酸反应及后续实验的一体化新设计
作者: 赵益汝 阎润鸿 冯高峰
摘 要: 综合各版本教材中铜与浓、稀硝酸反应实验及相关文献,设计铜和硝酸反应及其后续实验的一体化新装置。新装置使铜与硝酸在无氧条件下反应,有效解决了铜与稀硝酸反应生成的NO立刻被装置中的氧气氧化的问题。改进装置可一体化用于铜与浓硝酸、铜与稀硝酸、NO与氧气、NO2与水反应的四个实验,还可拓展用于其他需要无氧环境的液液反应和固液反应实验。
关键词: 装置一体化; 铜与硝酸反应; 实验装置改进; 实验探究
文章编号: 10056629(2024)10007203
中图分类号: G633.8
文献标识码: B
1 问题提出
氮及其化合物是高中化学阶段无机化学中重要的非金属元素,氮氧化物的制备、性质及其转化是高中化学重要的实验之一。《普通高中化学课程标准(2017年版)》中将“氮氧化物的转化”和“浓、稀硝酸的性质”写入了“常见无机物及其应用”主题学习活动建议的实验中,主题“常见的无机物及其应用”的内容要求中也建议通过实验探究了解氮及其重要化合物的主要性质[1]。现行各版本的高中化学教材也都编排了铜与浓、稀硝酸发应的实验,除了表述形式与实验装置等略有不同外,也都存在一定的不足之处。
对于铜和硝酸反应的实验改进,文献大多集中于铜与浓稀硝酸反应一体化,以解决实验的污染和安全问题。黎佩茹[2]将浓硝酸稀释为稀硝酸,在同一装置中完成了铜与浓、稀硝酸的反应,但该装置中的空气并未排出,根据现象,学生容易误认为铜与稀硝酸反应直接生成了红棕色的二氧化氮。赵立胜等[3]利用双注射器巧妙结合了铜和不同浓度硝酸的反应,但该实验存在装置复杂、不易操作等问题;姚亮发等[4]完成了铜与稀硝酸的反应,一定程度上排除了氧气的干扰,但缺少了铜与浓硝酸反应的重要实验。
化学实验是课堂教学中培养学生核心素养的重要载体。如铜与稀硝酸反应的产物是NO,进而演示NO氧化得到NO2,这对于学生科学探究与创新意识、证据推理与模型认知等核心素养的培养具有不可替代的作用。基于此,本文设计了一套铜与浓、稀硝酸反应的一体化实验装置,充分说明稀硝酸与铜反应的产物为NO;利用三通阀和氮气球实现NO2与水的反应,并解决了尾气污染等问题。
2 铜与硝酸反应及后续实验的一体化新设计
2.1 实验原理
NO极易被氧化,装置中需要去除氧气。新设计利用抽气泵和氮气球,通过“抽气回充氮气”的方法,实现无氧的反应环境。利用三通阀和氧气球,为氧化NO提供氧气,验证铜与稀硝酸反应产生的气体为NO,NO与O2反应才生成红棕色NO2。用氧气替代空气可增加实验的严谨性,有效落实证据推理化学核心素养的培养。
2.2 实验仪器及试剂
实验仪器:真空隔膜泵(西安双尺戒仪器有限公司,型号:BT15T)、恒压滴液漏斗(50mL)、三颈圆底烧瓶(19#磨口,100mL)、烧杯(200mL)、集气瓶(200mL)、橡胶塞、漏斗、球型干燥管、气球
实验试剂及用品:NaOH溶液(0.5mol/L)、浓硝酸(63%,3.5mL)、稀硝酸(浓硝酸3.5mL和水14mL混合物)、铜粉(2.0g)、氧气球、氮气球、三通阀、蒸馏水、石蕊
2.3 实验装置
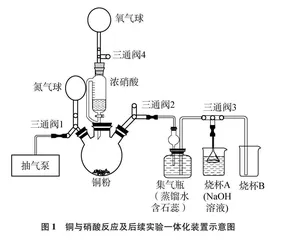
新设计的实验装置如图1所示(夹持装置略)。抽气装置采用小型实验室用抽气泵,配合氮气球可实现三颈圆底烧瓶无氧反应环境。一体化实验装置主要由抽气装置、反应发生装置、收集装置、尾气处理装置等组成。
2.4 实验步骤及现象
(1) 检查装置气密性。如图1所示安装好实验仪器,关闭恒压滴液漏斗旋塞,旋转三通阀2,联通三颈圆底烧瓶和玻璃管路;打开三通阀3,使之水平相通;打开三通阀1,将氮气球中的氮气充入烧瓶,观察集气瓶右侧水中玻璃管的液面是否上升,如上升说明装置气密性良好。
(2) 去除反应体系中的氧气。采用“抽气置换”法将反应体系中的空气置换为氮气。抽气前先在三颈圆底烧瓶中装入铜粉(2.0g),向恒压滴液漏斗加入浓硝酸(7.0mL),上口接三通阀4、三通阀4接氧气球(所连三通阀4为关闭状态)。具体操作为:关闭三通阀2、三通阀3和恒压滴液漏斗,通过抽气泵和旋转三通阀1将烧瓶中的空气抽走;然后旋转三通阀1向三颈圆底烧瓶中充入氮气(气流速率不宜过快,容易将铜粉吹散);重复上述操作3次,将反应体系(三颈圆底烧瓶和恒压滴液漏斗)中的空气置换成氮气,最后关闭三通阀1。
(3) 铜与浓硝酸反应。首先,旋转三通阀2,联通反应管路,然后旋转三通阀3使之水平相通。打开恒压滴液漏斗旋塞,将浓硝酸滴入圆底烧瓶,并通过旋转活塞控制浓硝酸滴入速度和量(3.5mL),观察到铜粉表面有气泡产生,烧瓶中马上充满红棕色气体——NO2。
(4) NO2与水反应。验证NO2与水反应生成硝酸和NO。具体操作为:旋转三通阀1,让氮气充入圆底烧瓶,直至将红棕色气体全部通过管路通入含有石蕊的蒸馏水中,水变红色(说明集气瓶中发生NO2与水反应生成酸性物质,酸性物质使石蕊变红)。同时液体被气体压至烧杯B。旋转三通阀3,将多余的红棕色NO2压至烧杯A中用NaOH溶液吸收;关闭三通阀1,停止通入氮气。打开三通阀4,使氧气充入反应体系,圆底烧瓶、管路和集气瓶上方均出现红棕色气体。说明NO2与水反应生成酸性物质外,还生成NO气体。根据NO2的化合价和产物NO的化合价,我们推测酸性物质为硝酸(化合价歧化),即反应的方程式为:3NO2+H2O2HNO3+NO。关闭氧气,打开三通阀1,用氮气将红棕色NO2气体压入烧杯A中继续用NaOH溶液吸收。
(5) 铜与稀硝酸反应。用注射器快速向恒压滴液漏斗注入水(14mL)将剩余浓硝酸(3.5mL)稀释为稀硝酸。重复步骤(2),将体系中的氧气置换为氮气。打开恒压滴液漏斗旋塞,调节并控制滴入的稀硝酸,可以观察到有气泡产生,但无有色气体生成。
(6) NO的氧化。旋转三通阀3,联通烧杯A;旋转氧气球所连三通阀4,将气球中的氧气与恒压滴液漏斗和三颈圆底烧瓶联通,可观察到三颈圆底烧瓶出现了红棕色气体,即生成了NO2。
(7) 尾气吸收。升高蒸馏水集气瓶中右侧导管,旋转三通阀2,使管路相通,氧气可继续压入三颈圆底烧瓶,将红棕色的NO2气体排入烧杯A中用NaOH溶液吸收,直至装置内无红棕色气体。反应的方程式为:4NO2+O2+4NaOH4NaNO3+2H2O。
3 小结
本改进实验具有以下优点:
(1) 一体化整合:将Cu与浓硝酸反应生成NO2,Cu与稀硝酸反应生成NO,NO与O2反应生成NO2,NO2与H2O反应生成HNO3和NO四个教学实验整合为一体,教师可根据教学进度来安排演示实验,实现一次投料,分步、有序进行多个实验的目的。
(2) 实验操作易控:恒压滴液漏斗带有刻度,可有效控制硝酸用量和滴加速度,进而控制反应进行,方便实验展示,提高教学效果。
(3) 无氧条件:设计的“抽气回充氮气”方法,能达到一般的无氧条件,可以适用于其他需要无氧条件下的固液反应和液液反应。
参考文献:
[1]中华人民共和国教育部制定. 普通高中化学课程标准(2017年版) [S]: 北京: 人民教育出版社, 2018.
[2]黎佩茹. 铜与硝酸反应装置的改进[J]. 中学化学教学参考, 2020, (13): 44~45.
[3]赵立胜, 李德前. 铜与浓、稀硝酸反应实验的新设计[J]. 中国现代教育装备, 2017, (24): 43~44.
[4]姚亮发, 郑柳萍, 张贤金等.基于证据推理意识的铜与稀硝酸反应实验的新设计[J]. 化学教学, 2022, (12): 75~77.