有机化学基础模块中“结构决定性质”观念建构教学探索
作者: 卓峻峭
摘 要: 新课程体系中建构“结构决定性质”核心观念对促进模块融合、发展核心素养和转变学习方式有重要意义。建构“结构决定性质”观念的教学要充分研究教材内容,设计有效的课堂问题引导学生开展深层次的思维活动,从结构化学的视角认识有机物性质和有机反应规律,从而促进学生对学科本原性知识、观念和思想的深刻理解和灵活应用。
关键词: 观念建构; 结构决定性质; 有机化学; 问题驱动
文章编号: 10056629(2024)10003007
中图分类号: G633.8
文献标识码: B
1 观念建构教学的价值和流程
1.1 观念建构教学及其价值
观念是指人们在实践活动中,通过总结和凝练形成对事物的本质和变化规律的认识,以及所获得的方法和价值等,具有可迁移性和持久性,显性或隐性地影响着人们的思维方式和价值取向。化学学科观念是学习者通过深入思考和内心体验形成的对化学知识和学科特征的理解和认识,可以通过化学教学建构[1~3]。
化学观念的建构能够将静态呈现的化学知识转为动态的有效迁移和应用,已成为化学教学的一个基本价值取向和实践追求[4]。实施观念建构教学主要有两个方面的价值:一是能引导学生认识知识点之间的内在联系,形成结构化的知识体系,有利于精简教学内容、转变学习方式、促进深度学习;二是能引导学生感悟化学知识中蕴含的思想、观点和方法,发挥核心观念对事实性知识的统摄和整合作用,形成化学学科的思想、观点和方法[5]。
1.2 观念建构教学流程
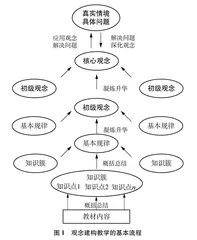
观念建构教学的基本流程可用图1表示。首先研读教材,对教学内容和事实材料进行深入的加工,精选具有代表性的相关知识点形成知识簇;接着概括总结出知识簇中蕴涵的基本规律,进一步凝练升华形成初级观念、核心观念;最后灵活地迁移、运用建构的观念解决具体的问题,此过程仍是在建构观念和深化观念,是观念建构教学不可或缺的组成部分。建构“结构决定性质”统摄性观念的过程具有阶段性和发展性,绝不是在某章某节的教学中一蹴而就的,而是需要贯穿于模块和学科的整体设计。
2 “结构决定性质”观念
2.1 “结构决定性质”的内涵
化学中对物质的研究可以分为物质的组成与结构和物质的性质与变化两个方面。在化学发展中,人们建立了从微观结构和宏观性质两个视角认识物质的思维模式,形成了“结构决定性质”的观念,即物质的微观结构决定宏观性质,结构是内因,性质是外显。“结构决定性质”是“宏观辨识与微观探析”核心素养的具体体现,是认识学科本原性问题的思维方式,是引领教学内容结构化的核心观念。
2.2 课程体系中“结构决定性质”的价值
在2017年改革前的课程体系中,结构化学核心知识长期缺位,元素化学和有机化学教学缺少核心观念引领,导致教学活动停留在罗列知识和机械记忆等较浅层面,学生对于物质的性质和反应规律往往“知其然而不知其所以然”。2017年颁布的课程标准(以下简称“新课标”)中物质结构与性质和有机化学基础一起成为选择性必修模块,元素电负性、价键理论、杂化轨道理论、键和分子的极性等结构化学核心知识的学习为建构“结构决定性质”核心观念奠定了基础。新课标中六次提及“结构决定性质”,并将其称为“基本观念”“核心观念”“统摄性观念”,足见其在课程体系中的重要性[6]。
有机化学中分子结构丰富、性质多样,是建构“结构决定性质”观念的重要载体。新课标明确要求“认识有机化合物分子中共价键的类型、极性及其与有机反应的关系,知道有机化合物分子中基团之间的相互影响会导致键的极性发生改变”[7],这些内容都指向“结构决定性质”观念的建构。
3 “结构决定性质”观念建构教学实践路径
3.1 提升教师对新课程体系中模块关系的认识水平
教师对课程内容的理解决定了教学设计与实施水平。新课程体系中,教师要站在课程整体设计的角度,从全新的视角提高对“化学反应原理”“物质结构与性质”“有机化学基础”模块之间关系的理解,而“结构决定性质”统摄性观念正是联系这三个模块的核心纽带。在有机化学基础模块教学中,既要用化学反应原理模块中形成的思路和视角认识有机物的转化关系,又要用物质结构与性质模块中微观结构的知识认识有机物的宏观性质,以建构“结构决定性质”核心观念为目标,方能推进课程理念落地生根。
3.2 树立师生核心观念引领知识内容结构化的意识
传统化学教学中往往存在通过罗列和陈述的方式讲授的知识多、散、杂的弊病,因而新课程课堂中教师要通过各级、各类观念引领的教学内容结构化,生成知识少而精、思维深且敏的课堂;学生也要积极地在观念引领下通过深度思考从本质上认识和理解所学知识之间的关联性,不要过分关注知识的细节,形成知识结构化的学习方法。比如在学习有机化学模块伊始,教师就要有意识地引导学生从“键的极性”概念出发,建立“非极性键一般发生均裂,强极性键容易发生异裂”的认识视角和思维方式;再如学生从αH活性的角度学习羟醛缩合反应后,认识到“吸电子基团活化αH”的规律,进而从电子效应的视角理解酯缩合反应等的同类型缩合反应。
3.3 精选代表性教学内容促进核心观念的自然建构
适合建构“结构决定性质”核心观念或某一初级观念的教学内容往往分散在教材多个章节中。教师在备课时需理清教材知识脉络,明晰该节课欲建构的观念,精选教学内容和情境素材,甚至可以打破教材中原有的章、节框架和顺序,增强观念建构教学的指向性和有效性。比如在某有机物物理性质溶解性的教学中,可以利用“相似相溶”原理,在一节课内全面分析烃、卤代烃、醇、酚、醛、酮、羧酸及其衍生物等有机物的溶解度(性),形成学生对溶解度(性)规律的全面认识和理解,促进“结构决定性质”核心观念的建构。
3.4 利用有思考价值的问题激发学生高阶思维活动
问题是思维的源泉和动力,是课堂教学中师生互动的主要方式。课堂教学过程中,要在挖掘教材内容的基础上,设计识记性问题和思考性问题,激发学生基于已有知识开展深层次思维活动,提高学生头脑中知识的整体性和概括性水平;同时根据学生回答情况了解和评价学生知识掌握及观念建构水平,及时调整教学策略,保证教学质量。
4 “结构决定性质”观念建构教学的具体实施:内容分析和问题设计
教材内容分析和课堂问题设计是实施观念建构教学的两个重要而具体的环节。本节从“共价键结构决定有机物性质”和“有机分子中原子、基团之间存在影响”两个最具代表性的初级观念出发,基于教材内容设计驱动性问题,生成观念建构课堂。
4.1 共价键结构决定有机物性质
化学反应是旧化学键断裂和新化学键形成的过程,有机反应亦是如此。有机反应中涉及的化学键以共价键为主,共价键的性质决定了有机物的反应性质,从共价键的视角认识有机物性质、分析有机反应性质是学习有机化学必备的思维方式[8]。基于图1中观念建构教学流程,“共价键结构决定有机物性质”观念的内容分析和建构逻辑如图2所示。
4.1.1 共价键的性质决定有机物的反应性质
4.1.1.1 教材内容分析
新教材介绍了σ键和π键的结构特点和反应规律,相关内容见表1。
4.1.1.2 教学活动设计
[问题1](烯烃、炔烃)为什么乙烯、乙炔可以使酸性KMnO4溶液退色而乙烷不能?
[分析]乙烯的碳碳双键、乙炔的碳碳三键中都既有σ键又有π键,乙烷的碳碳单键中只有σ键。σ键中电子云头碰头重叠程度大而稳定,π键中电子云肩并肩重叠程度较小而不稳定。
[问题2](卤代烃)测定结果表明C—Cl键键
长顺序为:一氯乙烷(C2H5Cl)>一氯乙烯(C2H3Cl)>一氯乙炔(C2HCl)。给出合理的解释。
[分析]一方面,三种分子中形成C—Cl键的C原子杂化轨道不同,杂化轨道中s成分越多,形成的C—Cl键越强,键长越短;另一方面,原子间形成π键会使键长变短,一氯乙炔中C(sp)与Cl原子形成两个π43,一氯乙烯中C(sp2)与Cl原子形成一个π43,而一氯乙烷中C(sp3)无法形成π43。
[问题3](卤代烃)溴乙烷在50℃时即能与NaOH溶液发生水解反应,而溴苯需要在高温、高压和催化剂的条件下才能发生水解反应。给出合理解释。
[分析]溴乙烷中C—Br键是sp3杂化,C原子形成普通的σ键;而溴苯中溴原子p轨道电子可与苯环共轭形成π键,其中sp2杂化的C原子形成的C—Br键的性质介于单键和双键之间,键能更大,更难断裂,水解反应条件更苛刻。
[问题4](合成高分子的基本方法)在苯乙烯的聚合反应中,利用C6H5CH2X做引发剂,生成自由基C6H5CH2·,实现苯乙烯的可控聚合。比较C6H5CH2Cl、 C6H5CH2Br和C6H5CH2I生成自由基反应的活性强弱。
[分析]Cl、 Br、I分别用3p、 4p、 5p轨道与C原子成键,原子轨道半径依次增大,成键时轨道重叠程度和键能依次减小,活性强弱顺序为:C6H5CH2I>C6H5CH2Br>C6H5CH2Cl。
4.1.2 键合原子电负性影响共价键性质
4.1.2.1 教材内容分析
新教材从卤代烃开始就利用结构化学知识逐步建构“键合原子电负性影响共价键性质”的初级观念,并应用此观念分析醇和羧酸的性质和反应位点,预测不对称加成反应的产物结构,实现了建构观念和运用观念的有机融合(见表2)。
4.1.2.2 教学活动设计
[问题5](研究有机化合物的一般方法)乙醇和乙醚互为同分异构体,如何鉴别二者?
[分析]乙醇的羟基中有强极性的O—H键(电负性差值1.4)易断裂,能与Na反应产生氢气;而乙醚中只有弱极性的C—H键(电负性差值0.4),不能与Na反应产生氢气。
[问题6](醛、酮)乙醛与HCN的加成反应中,加入少量的NaOH可以加快反应速率。给出合理的解释。
[分析]NaOH可将HCN转化为CN-,其中带负电的C原子更容易与乙醛中带正电的C原子成键。
[问题7](醛、酮)甲醛能与蛋白质分子中的氨基反应致使蛋白质变性。预测RNH2与HCHO发生加成反应的产物。
[分析]RNH2中强极性的N—H键易断裂,其中带负电的N原子与醛基中带正电的C原子成键,带正电的H原子与醛基中带负电的O原子成键,加成反应产物为
。
[问题8](有机合成)阐释卤代烃在有机合成中举足轻重的“桥梁”地位。
[分析]有机合成的原料主要为来自石油中的烃类,反应活性不高。将烃转化为卤代烃后,由于卤素原子电负性大于碳原子,使C—X键具有较强极性而易发生断裂,与试剂的基团结合生成新的化合物。
[问题9](有机合成)写出CH3CN在NaOH溶液中水解的产物。
[分析]CN中C原子呈正电性而N原子呈负电性,水解时C原子与OH-结合而N原子与H+结合,发生如下反应:
最终水解产物为CH3COONa和NH3。
[问题10](高分子材料)高分子材料中,聚乙烯、聚丙烯很难降解,而聚乙二醇容易降解。给出合理的解释。
[分析]聚乙烯、聚丙烯的高分子主链中是非极性(或弱极性)的C—C键,不易断裂;而聚乙二醇中有极性较强的C—O键,容易断裂而降解。
4.2 有机分子中原子、基团之间存在影响
有机分子是多种原子、原子团通过共价键作用聚集形成的整体,处于整体中的各要素之间存在相互影响,结果导致一些原子的电性和共价键的极性发生变化,进而影响其反应性质[15,16]。基于图1中观念建构教学流程,“有机分子中原子、基团之间存在影响”观念的内容分析和建构逻辑如图3所示。